题目内容
【题目】随着经济的发展,能源、环境、材料成为人们日益关注的问题:
(1)倡导“低碳”生活,保护环境,下列举措能达到“低碳”目的是_________。
A.提倡使用节能灯 B.广泛使用一次性筷子
C.利用和开发太阳能、风能等能源 D.选择步行、骑自行车等方式出行
(2)天然气(主要成分是CH4)是家庭常用的燃料。若32g CH4 完全燃烧,至少需要氧气的质量是___________已知标准状况下,氧气的密度是1.4g/L,则在标准状况下,32g CH4 完全燃烧,理论上需要空气多少升?(计算结果保留一位小数,写出计算过程)_________
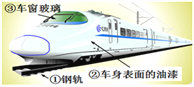
(3)高速铁路可以加快出行步伐。结合所学化学知识,回答下列问题:
I、图中标示的物质中为金属材料的是_________(填序号),动车表面喷漆主要是为了防止外壳生锈,其原理是_________。
II、修建铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得。下列矿石的主要成分属于氧化物的是_________(填字母序号);
A.铝土矿 (主要成分A12O3) B.辉铜矿(主要成分Cu2S)
C.菱铁矿 (主要成分FeCO3) D.磁铁矿 (主要成分Fe3O 4)
III、高铁酸钠(Na2FeO4)是高铁列车上常用的一种“绿色环保高效”消毒剂。高铁酸钠中铁元素化合价为_________。
(4)将一定质量的锌粒投入含有Cu(NO3)2和Fe(NO3)2的混合溶液中,充分反应后过滤,若滤液中只含一种溶质,则滤渣中一定含有_________。
【答案】A、C、D 128g 457.1L ① 阻碍了铁与氧气和水接触 AD +6价 铜和铁(Cu和Fe)
【解析】
(1)提倡低碳经济的措施有:提倡使用节能灯;利用和开发太阳能、风能等能源;选择步行、骑自行车、乘坐公共交通工具等方式出行等;广泛使用一次性筷子、一次性塑料袋不能达到“低碳”目的,故选ACD;
(1)甲烷中碳元素的质量分数为![]() ;
;
(2)设完全燃烧16g甲烷,最少需要氧气的质量为x,
CH4+2O2![]() CO2+2H2O
CO2+2H2O
16 64
32gx
![]() ,
,![]() =128g,则需空气的体积为
=128g,则需空气的体积为![]() ;(3)I、钢轨是由金属材料制成的;铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果,动车表面喷漆主要是为了防止外壳生锈,其原理是隔绝水和氧气(或空气);II、氧化物是由两种元素组成,其中一种是氧元素的物质,故铝土矿 (主要成分A12O3)、磁铁矿 (主要成分Fe3O 4)均属于氧化物;III、在Na2FeO4中,Na元素的化合价为+1价,O元素的化合价为-2价,
;(3)I、钢轨是由金属材料制成的;铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果,动车表面喷漆主要是为了防止外壳生锈,其原理是隔绝水和氧气(或空气);II、氧化物是由两种元素组成,其中一种是氧元素的物质,故铝土矿 (主要成分A12O3)、磁铁矿 (主要成分Fe3O 4)均属于氧化物;III、在Na2FeO4中,Na元素的化合价为+1价,O元素的化合价为-2价,
设该化合物中Fe元素的化合价为x,由化学式和化合物中正负化合价的代数和为0,则
(+1)×2+x+(-2)×4=0解得x=+6;(4)由于金属的活动性大小是:锌>铁>铜,将一定质量的锌粒投入含有Cu(NO3)2和Fe(NO3)2的混合溶液中,锌先与硝酸铜反应生成了硝酸锌和铜,当硝酸铜完全反应后锌再与硝酸亚铁反应生成了硝酸锌和铁,充分反应后过滤,若滤液中只含一种溶质,应该是硝酸锌,所以滤渣中一定含有铜、铁。

【题目】小明想测定Cu-Fe合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀硫酸和相关仪器。
(1)根据现有的条件,你认为只能测出________合金中铜的质量分数。
(2)为了测定该合金的组成,小明称取20g该合金粉末,将80g稀硫酸分两次加入粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 | 第二次 | |
连续加入稀硫酸的质量(g) | 40 | 40 |
生成氢气的质量(g) | 0.3 | 0.1 |
从上表数据分析,小明用20g合金粉末总共收集到氢气_________g。
(3)求出该合金中铜的质量分数为_________。(写出具体计算过程)