题目内容
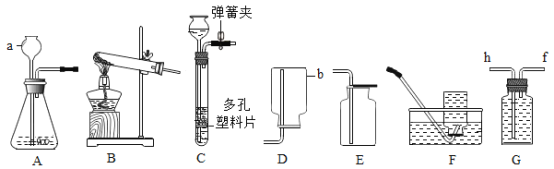
【题目】如图所示是实验室制取气体的常用装置,请根据要求回答问题:
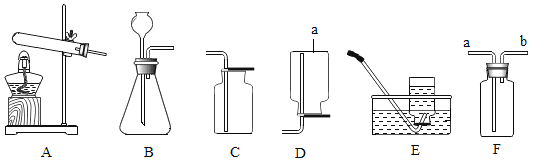
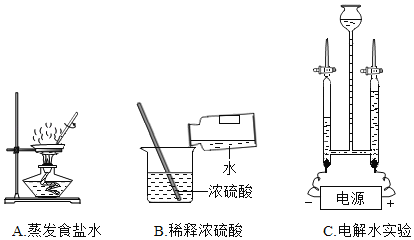
(1)仪器 a的名称是_____;利用装置 A 制取氧气时,反应的文字表达式是__________________;
(2)若用分解过氧化氢制取干燥的氧气,应选择的发生装置为_________,收集装置为______________,锥形瓶内长颈漏斗要插入液面以下,其原因是 _________________________ ;若想要控制反应的速率,应将__________________。
(3)若实验是用高锰酸钾制取并收集纯净的氧气,应选择的装置为_________,应该对发生装置做何改进___________________,目的是___________,文字表达式为_______________。 若用 F 来收集氧气,氧气从哪端进_____________ ,验证氧气是否收集满的方法是__________________________。
(4)已知:氨气(NH3)是一种具有刺激性气味的无色气体,密度比空气小,极易溶于水,实验室常用加热氯化铵和熟石灰两种固体的混合物来制备氨气。请你从图中选出制备一瓶氨气所需要的装置组合是_____。
【答案】集气瓶 氯酸钾![]() 氯化钾+氧气 B C 防止氧气从长颈漏斗逸出 长颈漏斗换成分液漏斗 AE 试管口需要放一团棉花 防止高锰酸钾粉末进入导管 高锰酸钾
氯化钾+氧气 B C 防止氧气从长颈漏斗逸出 长颈漏斗换成分液漏斗 AE 试管口需要放一团棉花 防止高锰酸钾粉末进入导管 高锰酸钾![]() 锰酸钾+二氧化锰+氧气 a 将带火星的木条放在b导管口,木条复燃,证明集满 AD
锰酸钾+二氧化锰+氧气 a 将带火星的木条放在b导管口,木条复燃,证明集满 AD
【解析】
(1)通过分析题中所指仪器的名称和作用可知,a是集气瓶;
氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,文字表达式为:氯酸钾![]() 氯化钾+氧气;
氯化钾+氧气;
(2)实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,向上排空气法收集的氧气干燥,所以应选择的发生装置为B,收集装置为C,锥形瓶内长颈漏斗要插入液面以下,其原因是:防止氧气从长颈漏斗逸出,分液漏斗可以控制液体的滴加速度,所以想要控制反应的速率,应该将长颈漏斗换成分液漏斗;
(3)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,排水法收集的氧气纯净,所以应选择的装置为AE,试管口需要放一团棉花,目的是:防止高锰酸钾粉末进入导管,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,文字表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气,氧气密度比空气大,有助燃性,所以用F来收集氧气,氧气从a端进,验证氧气是否收集满的方法是:将带火星的木条放在b导管口,木条复燃,证明集满;
锰酸钾+二氧化锰+氧气,氧气密度比空气大,有助燃性,所以用F来收集氧气,氧气从a端进,验证氧气是否收集满的方法是:将带火星的木条放在b导管口,木条复燃,证明集满;
(4)实验室制取氨气的反应物是固体,反应条件是加热,氨气密度比空气小,极易溶于水,所以选出制备一瓶氨气所需要的装置组合是AD。
故答案为:
(1)集气瓶;氯酸钾![]() 氯化钾+氧气;
氯化钾+氧气;
(2)B,C,防止氧气从长颈漏斗逸出,长颈漏斗换成分液漏斗;
(3)AE,试管口需要放一团棉花,防止高锰酸钾粉末进入导管,高锰酸钾![]() 锰酸钾+二氧化锰+氧气,a,将带火星的木条放在b导管口,木条复燃,证明集满;
锰酸钾+二氧化锰+氧气,a,将带火星的木条放在b导管口,木条复燃,证明集满;
(4)AD。

 阅读快车系列答案
阅读快车系列答案【题目】已知二氧化锰能作过氧化氢分解的催化剂,某兴趣小组想探究其他物质是否也可以作过氧化氢分解的催化剂。请参与他们的探究过程。
(提出问题)
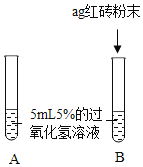
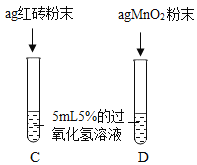
红砖粉末能否作为过氧化氢分解的催化剂?如果能,效果如何?
(进行实验)
实验步骤 | 实验现象 | 实验结论及解释 |
Ⅰ. | A中无明显现象,B中产生大量能使带火星木条复燃的气体 | ①产生的气体是_____; |
Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ①又产生大量能使带火星木条复燃的气体 | 红砖粉末的_____和_____在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
Ⅲ. | 两试管中均产生气泡,不同之处是加入二氧化锰的试管中产生气泡的速率比加入红砖粉末的_____(填“快”或“慢”) | 红砖粉末的催化效果没有二氧化锰粉末好 |
(得出结论)
故红砖粉末能作过氧化氢分解的催化剂。写出红砖粉末催化过氧化氢分解反应的文字表达式_____;
(拓展延伸)
下列有关催化剂的说法正确的是_____(填字母)。
A 催化剂只能加快反应速率
B 催化剂不能决定反应能否发生
C 使用催化剂能增加产物质量