题目内容
【题目】取25 g大理石与200 g稀盐酸恰好完全反应。反应过程中剩余固体的质量与反应时间的关系如下表:
反应时间/s | t1 | t2 | t3 | t4 |
剩余固体的质量/g | 20 | 10 | 5 | 5 |
试完成以下计算:
(1)25 g样品中含碳酸钙的质量为_______g。
(2)反应后生成氯化钙的质量_______。
(3)反应后溶液中溶质的质量分数为多少_______?
【答案】20 8.8g 10.5%
【解析】
(1)根据表中的数据分析大理石中含碳酸钙的质量,根据碳酸钙的质量求出共生成二氧化碳的质量;
(2)根据上述计算求出生成的氯化钙的质量;
(3)根据溶质质量分数的计算公式计算。
解:(1)根据表中的数据可知,大理石中杂质的质量为5g,含碳酸钙的质量为:25g-5g=20g;
(2)设生成的氯化钙的质量为x,生成的二氧化碳的质量为y,

![]() x=22.2g,
x=22.2g,
![]() y=8.8g,
y=8.8g,
(3)反应后溶液的溶质质量分数为:![]() ×100%=10.5%;
×100%=10.5%;
答:(1)25 g样品中含碳酸钙的质量为20g;
(2)反应后生成氯化钙的质量22.2g;
(3)反应后溶液的溶质质量分数为10.5%。

【题目】钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)高科技产品“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的_________。
II.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:__________________;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能______________;
Ⅲ.铁的活动性探究
现用一定量的AgNO3和Cu (NO3)2混合溶液,进行了如图所示的实验,并对溶液A和固体B的成分进行了分析和研究.
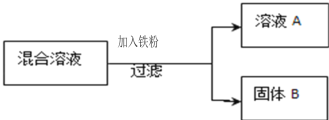
(提出问题)溶液A中的溶质可能有哪些?
(作出猜想)
①只有Fe(NO3)2
②有Fe (NO3)2、Cu (NO3)2
③ 有Fe (NO3)2、AgNO3
④ 有Fe (NO3)2、Cu (NO3)2、AgNO3
(交流讨论)不合理的猜想是__(填标号),其理由是_______
(实验探究)根据如表中的实验步骤及现象,完成表中的实验结论
实验步骤 | 现象 | 实验结论 |
取少量固体B,滴加 稀盐酸 | 有气泡产生 | 溶液A中的溶质成分符合 猜想_____.固体B中的金属成分是________. |
Ⅳ.生铁中铁含量的测定
某课外兴趣小组测定生铁(含杂质的铁,杂质既不溶于水也不溶于酸)中铁的质量分数,他们取五份样品,分别加稀硫酸反应.测得部分数据如下,请根据有关信息回答问题.
实验次数 | 1 | 2 | 3 | 4 | 5 |
取样品质量(g) | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 |
取稀硫酸质量(g) | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
产生气体质量(g)/span> | 0.2 | a | 0.6 | 0.8 | 0.9 |
(1)a的数值为______.
(2)列式计算该样品中单质铁的质量分数______.
(3)第5次实验结束后,所得到溶液中溶质的化学式为_______.
(4)第1次实验结束后,所得到溶液中溶质质量分数______?列式计算写过程。