题目内容
在学习了“复分解反应发生的条件”的知识后,某化学兴趣小组将一定量的碳酸钠溶液和氯化钡溶液混合时,发现产生了白色沉淀,将沉淀过滤后得到滤液.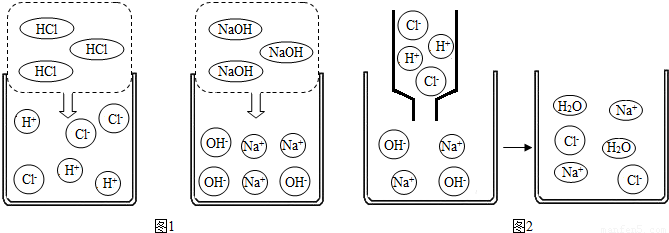
[实践运用]根据复分解反应的知识,该反应的化学反应方程式为:______.
[挖掘实质]
(1)图1是HCl和NaOH在水中解离出离子的示意图,小丽发现HCl在水中会解离出H+和Cl-,NaOH在水中会解离出Na+和OH-,以此类推硝酸铜在水中会解离出的离子是______(填离子符号)______.
(2)图2是稀盐酸和氢氧化钠溶液发生化学反应的微观过程示意图,该化学反应的实质可以表示为:H++OH-=H2O
我也能用同样的方式表示碳酸钠溶液与氯化钡溶液之间发生反应时有沉淀生成的反应实质______.
[猜想与假设]该小组对滤液中溶质的成分作出了两种合理的假设.
假设①:溶质为NaCl
假设②:溶质为NaCl、BaCl2
请你再补充一种合理的假设.
假设③:溶质为______.
[实验探究]如果假设③成立,请你根据下表实验方案,完成空格.
| 实验步骤及操作方法 | 实验现象 | 结 论 |
| a、向装有滤液的烧杯中滴加 硝酸银溶液 | ______ | 假设③成立 |
| b、过滤后,向白色沉淀中加入足量的______. | 白色沉淀部分溶解,且有 ______产生 |
【答案】分析:[实践运用]根据碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠进行解答;
[挖掘实质](1)根据硝酸铜在水中会解离出铜离子和硝酸根离子进行解答;
(2)根据碳酸钠溶液与氯化钡溶液之间发生反应时有沉淀生成的反应实质是钡离子和碳酸根离子结合生成碳酸钡沉淀进行解答;
[猜想与假设]根据碳酸钠溶液与氯化钡溶液之间发生反应量的不同进行解答;
[实验探究]根据硝酸银溶液和氯化钠溶液反应会生成氯化银白色沉淀以及硝酸银溶液和碳酸钠溶液反应会生成碳酸银白色沉淀进行解答;
[小结]根据Na2CO3和 BaCl2恰好完全反应,溶质只有氯化钠进行解答.
解答:解:[实践运用]碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,反应的化学反应方程式为:Na2CO3+BaCl2═BaCO3↓+2NaCl;
[挖掘实质](1)硝酸铜在水中会解离出铜离子和硝酸根离子,离子符号Cu2+、NO3-;
(2)碳酸钠溶液与氯化钡溶液之间发生反应时有沉淀生成的反应实质是钡离子和碳酸根离子结合生成碳酸钡沉淀,可以表示为:Ba2++CO32-═BaCO3↓;
[猜想与假设]当碳酸钠溶液与氯化钡溶液恰好发生时,溶质为NaCl;当氯化钡溶液有剩余时,溶质为NaCl、BaCl2;当碳酸钠溶液有剩余时,溶质为NaCl、Na2CO3;
[实验探究]硝酸银溶液和氯化钠溶液反应会生成氯化银白色沉淀,硝酸银溶液和碳酸钠溶液反应会生成碳酸银白色沉淀,而氯化银不溶于稀硝酸,碳酸银溶于硝酸,会放出二氧化碳气体;
[小结]当Na2CO3和 BaCl2恰好完全反应,溶质只有氯化钠.
故答案为:【实践运用】Na2CO3+BaCl2═BaCO3↓+2NaCl;
【挖掘实质】(1)Cu2+;NO3-;(2)Ba2++CO32-═BaCO3↓;
【猜想与假设】溶质为NaCl、Na2CO3;
【实验探究】有白色沉淀产生;稀硝酸;气泡;
【小结】Na2CO3和 BaCl2恰好完全反应.
点评:要理解和熟记复分解反应的条件与实质,熟记常见酸、碱、盐的溶解性表,并能正确地运用物质的溶解性,方能顺利解题.
[挖掘实质](1)根据硝酸铜在水中会解离出铜离子和硝酸根离子进行解答;
(2)根据碳酸钠溶液与氯化钡溶液之间发生反应时有沉淀生成的反应实质是钡离子和碳酸根离子结合生成碳酸钡沉淀进行解答;
[猜想与假设]根据碳酸钠溶液与氯化钡溶液之间发生反应量的不同进行解答;
[实验探究]根据硝酸银溶液和氯化钠溶液反应会生成氯化银白色沉淀以及硝酸银溶液和碳酸钠溶液反应会生成碳酸银白色沉淀进行解答;
[小结]根据Na2CO3和 BaCl2恰好完全反应,溶质只有氯化钠进行解答.
解答:解:[实践运用]碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,反应的化学反应方程式为:Na2CO3+BaCl2═BaCO3↓+2NaCl;
[挖掘实质](1)硝酸铜在水中会解离出铜离子和硝酸根离子,离子符号Cu2+、NO3-;
(2)碳酸钠溶液与氯化钡溶液之间发生反应时有沉淀生成的反应实质是钡离子和碳酸根离子结合生成碳酸钡沉淀,可以表示为:Ba2++CO32-═BaCO3↓;
[猜想与假设]当碳酸钠溶液与氯化钡溶液恰好发生时,溶质为NaCl;当氯化钡溶液有剩余时,溶质为NaCl、BaCl2;当碳酸钠溶液有剩余时,溶质为NaCl、Na2CO3;
[实验探究]硝酸银溶液和氯化钠溶液反应会生成氯化银白色沉淀,硝酸银溶液和碳酸钠溶液反应会生成碳酸银白色沉淀,而氯化银不溶于稀硝酸,碳酸银溶于硝酸,会放出二氧化碳气体;
[小结]当Na2CO3和 BaCl2恰好完全反应,溶质只有氯化钠.
故答案为:【实践运用】Na2CO3+BaCl2═BaCO3↓+2NaCl;
【挖掘实质】(1)Cu2+;NO3-;(2)Ba2++CO32-═BaCO3↓;
【猜想与假设】溶质为NaCl、Na2CO3;
【实验探究】有白色沉淀产生;稀硝酸;气泡;
【小结】Na2CO3和 BaCl2恰好完全反应.
点评:要理解和熟记复分解反应的条件与实质,熟记常见酸、碱、盐的溶解性表,并能正确地运用物质的溶解性,方能顺利解题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目