题目内容
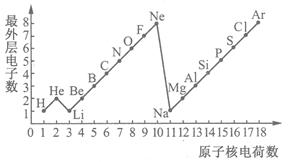
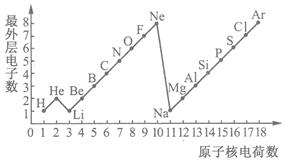
下图是1~18号元素原子最外层电子数与原子核电荷数的关系图.

请回答下列问题:
(1)l~18号元素中属于稀有气体元素的有
(2)He和Be元素的原子最外层均有2个电子,它们的化学性质是否相似?
(3)某元素的原子序数为16,它在化学反应中一般易

请回答下列问题:
(1)l~18号元素中属于稀有气体元素的有
He、Ne、Ar
He、Ne、Ar
(填元素符号).(2)He和Be元素的原子最外层均有2个电子,它们的化学性质是否相似?
不相似
不相似
.(填“相似”或“不相似”).(3)某元素的原子序数为16,它在化学反应中一般易
得到
得到
电子(填“得到”或“失去”),它与地壳中含量最多的金属元素形成化合物的化学式为Al2S3
Al2S3
.分析:(1)根据最外层电子数可分析稀有气体元素;
(2)根据原子结构来分析它们的性质是否相似;
(3)利用原子结构中的最外层电子数来分析其性质,地壳中含量最多的金属元素为铝元素,利用最外层电子数来分析其化合价,然后书写化学式.
(2)根据原子结构来分析它们的性质是否相似;
(3)利用原子结构中的最外层电子数来分析其性质,地壳中含量最多的金属元素为铝元素,利用最外层电子数来分析其化合价,然后书写化学式.
解答:解:(1)因有一个电子层时,电子数为2即为稳定结构,则He为稀有气体,有两个以上电子层时,最外层电子数为8的为稳定结构,由图可知则Ne、Ar为稀有气体,故答案为:He、Ne、Ar;
(2)因因He有一个电子层,则最外层电子数是2为稳定结构,化学性质稳定,但Be元素的原子有两个电子层,最外层电子数是2,则容易失去2个电子而满足稳定结构,化学性质较活泼,则它们的性质不相似,故答案为:不相似;
(3)因元素的原子序数为16的是S元素,其最外层电子数为6,则容易得到2个电子而满足最外层8电子的稳定结构,在化合物中化合价为-2价,而地壳中含量最多的金属元素为铝元素,其最外层电子数为3,容易失去最外层电子而满足最外层8电子的稳定结构,再化合物中的化合价为+3价,则
,由化合物中正负化合价的代数和为0,则化合价相互交叉,可得化学式为Al2S3,故答案为:Al2S3.
(2)因因He有一个电子层,则最外层电子数是2为稳定结构,化学性质稳定,但Be元素的原子有两个电子层,最外层电子数是2,则容易失去2个电子而满足稳定结构,化学性质较活泼,则它们的性质不相似,故答案为:不相似;
(3)因元素的原子序数为16的是S元素,其最外层电子数为6,则容易得到2个电子而满足最外层8电子的稳定结构,在化合物中化合价为-2价,而地壳中含量最多的金属元素为铝元素,其最外层电子数为3,容易失去最外层电子而满足最外层8电子的稳定结构,再化合物中的化合价为+3价,则
| +3 |
| Al |
| -2 |
| S |
点评:本题考查学生利用图中的最外层电子数来分析元素,并利用最外层电子数来分析性质,能利用化合价来书写物质的化学式,注重了化学用语的训练.

练习册系列答案
相关题目