题目内容
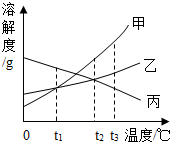 (2012?江宁区二模)如图为甲、乙、丙三种物质的溶解度曲线.下列说法正确的是( )
(2012?江宁区二模)如图为甲、乙、丙三种物质的溶解度曲线.下列说法正确的是( )分析:A、根据溶解度曲线可以比较同一温度下不同物质的溶解度大小;
B、根据溶解度曲线,选择分离、提纯某些可溶性混合物的方法(即选用蒸发结晶还是降温结晶);
C、根据溶解度曲线可以判断或比较析出晶体的质量大小(即曲线越陡,析出的晶体就越多).
D、根据乙的溶解度随温度升高而增大,丙的溶解度随温度升高而减小分析.
B、根据溶解度曲线,选择分离、提纯某些可溶性混合物的方法(即选用蒸发结晶还是降温结晶);
C、根据溶解度曲线可以判断或比较析出晶体的质量大小(即曲线越陡,析出的晶体就越多).
D、根据乙的溶解度随温度升高而增大,丙的溶解度随温度升高而减小分析.
解答:解:A、根据溶解度曲线可知:t1℃时甲、乙、丙三种物质的溶解度关系是甲=乙<丙,故A错误;
B、根据溶解度曲线可知:乙的溶解度随温度的升高逐渐增大,但变化不大,所以从乙饱和溶液中析出较多量的晶体最好采用蒸发结晶法,故B错误;
C、甲的溶解度随温度的升高而增大的幅度大,所以等质量的甲、乙饱和溶液从t3℃降温到t1℃,析出晶体(无结晶水)的质量甲>乙,故C正确;
D、乙的溶解度随温度升高而增大,丙的溶解度随温度升高而减小;故t2℃时,将乙、丙的饱和溶液升温至t3℃,乙溶液变为不饱和溶液,质量分数不变,丙溶液有溶质析出,质量分数减小,故D错误;
故选C.
B、根据溶解度曲线可知:乙的溶解度随温度的升高逐渐增大,但变化不大,所以从乙饱和溶液中析出较多量的晶体最好采用蒸发结晶法,故B错误;
C、甲的溶解度随温度的升高而增大的幅度大,所以等质量的甲、乙饱和溶液从t3℃降温到t1℃,析出晶体(无结晶水)的质量甲>乙,故C正确;
D、乙的溶解度随温度升高而增大,丙的溶解度随温度升高而减小;故t2℃时,将乙、丙的饱和溶液升温至t3℃,乙溶液变为不饱和溶液,质量分数不变,丙溶液有溶质析出,质量分数减小,故D错误;
故选C.
点评:掌握固体溶解度曲线的变化趋势及其作用;了解溶质的质量分数和溶解度的关系即可正确解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
