题目内容
农村经常使用氮肥硝酸铵(化学式为NH4NO3),今有一硝酸铵样品经过测定含氮量为37%,已知该化肥中只含有一种杂质,则该化肥中可能混有下列物质中的哪种氮肥
- A.氯化铵(NH4Cl)
- B.硫酸铵[(NH4)2SO4]
- C.尿素[CO(NH2)2]
- D.碳铵(NH4HCO3)
C
分析:首先计算纯净物硝酸铵中氮元素的质量分数,然后与样品中氮的质量分数相比,看谁的高.若样品中的高,则杂质中氮的质量分数必定高于硝酸铵中的;若样品中的低,则杂质中氮的质量分数必然低于硝酸铵中的;进行解答.
解答:纯净物硝酸铵中氮元素的质量分数=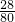 ×100%=35%
×100%=35%
A、氯化铵(NH4Cl)中氮元素的质量分数=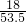 ×100%=26.2%
×100%=26.2%
B、硫酸铵[(NH4)2SO4]中氮元素的质量分数=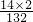 ×100%=21.2%
×100%=21.2%
C、尿素[CO(NH2)2]中氮元素的质量分数=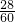 ×100%=46.7%
×100%=46.7%
D、碳铵(NH4HCO3)中氮元素的质量分数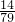 =×100%=17.8%
=×100%=17.8%
因为样品中含氮量为37%,纯净物硝酸铵中含氮量为35%,所以杂质中氮的质量分数必然高于硝酸铵中含氮量,
故选C.
点评:将质量分数的计算与生活实际相联系;再结合题意进行分析解答.
分析:首先计算纯净物硝酸铵中氮元素的质量分数,然后与样品中氮的质量分数相比,看谁的高.若样品中的高,则杂质中氮的质量分数必定高于硝酸铵中的;若样品中的低,则杂质中氮的质量分数必然低于硝酸铵中的;进行解答.
解答:纯净物硝酸铵中氮元素的质量分数=
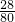 ×100%=35%
×100%=35% A、氯化铵(NH4Cl)中氮元素的质量分数=
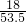 ×100%=26.2%
×100%=26.2%B、硫酸铵[(NH4)2SO4]中氮元素的质量分数=
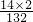 ×100%=21.2%
×100%=21.2%C、尿素[CO(NH2)2]中氮元素的质量分数=
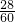 ×100%=46.7%
×100%=46.7%D、碳铵(NH4HCO3)中氮元素的质量分数
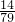 =×100%=17.8%
=×100%=17.8%因为样品中含氮量为37%,纯净物硝酸铵中含氮量为35%,所以杂质中氮的质量分数必然高于硝酸铵中含氮量,
故选C.
点评:将质量分数的计算与生活实际相联系;再结合题意进行分析解答.

练习册系列答案
相关题目
农村经常使用氮肥硝酸铵(化学式为NH4NO3),今有一硝酸铵样品经过测定含氮量为37%,已知该化肥中只含有一种杂质,则该化肥中可能混有下列物质中的哪种氮肥( )
| A、氯化铵(NH4Cl) | B、硫酸铵[(NH4)2SO4] | C、尿素[CO(NH2)2] | D、碳铵(NH4HCO3) |