题目内容
【题目】将Fe粉置于Ag(NO3)2和Zn(NO3)2的混合溶液中,待反应完毕后,所得金属中一定含有的是( )
A、 Fe B、Fe, Ag C、Fe, Ag, Zn D、Ag
【答案】D
【解析】
试题分析: 将Fe粉置于Ag(NO3)2和Zn(NO3)2的混合溶液中,只能与Ag(NO3)2反应置换Ag,故所得金属为Ag或Ag、Fe.则一定含有Ag.

练习册系列答案
相关题目
【题目】(7分)某同学做了如下图所示实验:
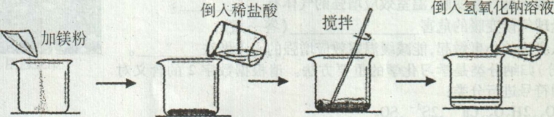
第一次 | 第二次 | |
加入镁粉的质量 | m | m |
加入质量分数为14.6%稀盐酸的质量 | 50g | lOOg |
加入氢氧化钠溶液的质量 | 100g | 100g |
加入氢氧化钠溶液后的实验现象 | 产生白色沉淀 | 无明显现象 |
第一次实验每步均恰好完全反应,请回答:
(1)写出第一次实验中发生反应的化学方程式___________________________;
(2)第二次反应后溶液中溶质的组成是___________________________;
(3)每次实验中加入镁的质量(m)为___________________________;
(4)求解第一次反应中生成气体的质量(X)的比例式为___________________________;
(5)若将第一次反应后溶液蒸发掉68.4g水后,则所得不饱和溶液中溶质的质量分数___________;
(6)若用36.5%的浓盐酸配制实验中所需稀盐酸,则需要加水的质量为_______________。