题目内容
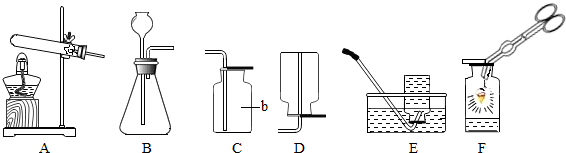
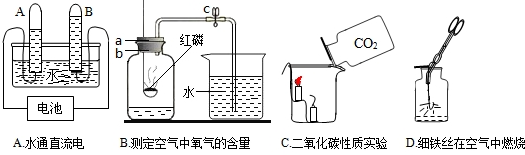
根据细铁丝在氧气中燃烧的实验,请回答下列问题:
(1)实验中观察到的现象是
(2)实验时要给铁丝系上一根火柴,其作用是
(3)瓶底要装有少量水,其作用是
(4)写出该反应的文字表达式
(5)若将氧气换成空气,则该反应
(1)实验中观察到的现象是
剧烈燃烧,火星四射,生成黑色固体,放出大量的热
剧烈燃烧,火星四射,生成黑色固体,放出大量的热
.(2)实验时要给铁丝系上一根火柴,其作用是
引燃铁丝
引燃铁丝
.(3)瓶底要装有少量水,其作用是
为了防止溅落的熔化物炸裂集气瓶底
为了防止溅落的熔化物炸裂集气瓶底
.(4)写出该反应的文字表达式
铁+氧气
四氧化三铁
| ||
铁+氧气
四氧化三铁
.
| ||
(5)若将氧气换成空气,则该反应
不能
不能
(填“能”或“不能”)进行,其原因是铁丝在空气中不能燃烧
铁丝在空气中不能燃烧
.分析:(1)根据铁丝在氧气中燃烧的实验现象分析问题;
(2)根据铁丝在氧气中燃烧的注意事项分析问题;
(3)根据反应物、生成物及反应条件写出反应的文字表达式;
(4)根据铁丝在空气中不能燃烧分析.
(2)根据铁丝在氧气中燃烧的注意事项分析问题;
(3)根据反应物、生成物及反应条件写出反应的文字表达式;
(4)根据铁丝在空气中不能燃烧分析.
解答:解:(1)铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,放出大量的热;
(2)实验时要给铁丝系上一根火柴,其作用是引燃铁丝;
(3)铁丝在氧气中燃烧时,为了防止溅落的熔化物炸裂集气瓶底,集气瓶内预留少量水;
(3)铁丝在氧气中燃烧生成了四氧化三铁,反应的文字表达式是:铁+氧气
四氧化三铁;
(4)由于铁丝在空气中不能燃烧,所以若实验将氧气换成空气,则该反应不能进行.
故答为:(1)剧烈燃烧,火星四射,生成黑色固体,放出大量的热;(2)为了防止溅落的熔化物炸裂集气瓶底;(3)铁+氧气
四氧化三铁;(4)不能;铁丝在空气中不能燃烧.
(2)实验时要给铁丝系上一根火柴,其作用是引燃铁丝;
(3)铁丝在氧气中燃烧时,为了防止溅落的熔化物炸裂集气瓶底,集气瓶内预留少量水;
(3)铁丝在氧气中燃烧生成了四氧化三铁,反应的文字表达式是:铁+氧气
| ||
(4)由于铁丝在空气中不能燃烧,所以若实验将氧气换成空气,则该反应不能进行.
故答为:(1)剧烈燃烧,火星四射,生成黑色固体,放出大量的热;(2)为了防止溅落的熔化物炸裂集气瓶底;(3)铁+氧气
| ||
点评:本题难度不大,掌握常铁丝在氧气中燃烧的现象即可正确解答;在描述燃烧的现象时,需要注意光和火焰、烟和雾的区别.

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目