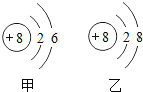
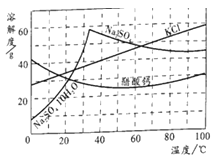
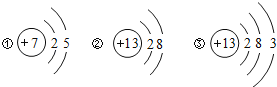题目内容
【题目】化学是一门实验科学,关注物质变化过程,探究物质变化的条件很有必要.某化学兴趣小组用如图所示的实验探究物质燃烧的条件.
回答下列问题:
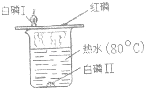
(1)实验中要严重可燃物燃烧的条件之一是与氧气接触,应观察到的现象是 .
(2)铜片上的白磷燃烧而红磷不燃烧,说明可燃物燃烧的另一条件是 .
(3)写出磷燃烧的化学方程式 .
【答案】(1)铜片上的白磷燃烧,水中白磷不燃烧;
(2)温度需要达到着火点;
(3)4P+5O2![]() 2P2O5
2P2O5
【解析】
试题分析:根据物质燃烧的条件:物质具有可燃性、与氧气接触、达到着火点,可知铜片上的红磷没有达到着火点,白磷达到着火点,并与氧气接触,水中的白磷达到着火点,但不与氧气接触,可以据此答题.
解:(1)由于铜片上的白磷与氧气接触,温度达到了它的着火点,所以能够燃烧;水中的白磷虽然温度达到了着火点,但没有与氧气接触,不能燃烧;
故填:铜片上的白磷燃烧,水中白磷不燃烧;
(2)白磷的着火点是40℃,红磷的着火点是240℃,薄铜片上的白磷燃烧而红磷不燃烧,说明物质燃烧,温度需要达到着火点;
故填:温度需要达到着火点;
(3)磷燃烧生成五氧化二磷,化学方程式为:反应的方程式为:4P+5O2![]() 2P2O5.
2P2O5.
故填:4P+5O2![]() 2P2O5
2P2O5

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案【题目】化学教材“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣.
【提出问题】(1)氧化铁能否作过氧化氢溶液分解的催化剂?
(2)氧化铁与二氧化锰催化效果哪个好?
【实验探究】
实验步骤 | 实验现象 |
①分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入a g氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象. | A试管中产生大量气泡,带火星木条复燃,B试管中的现象 |
②待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管内,如此反复多次实验,观察现象. | 试管中均产生大量气泡,带火星木条均复燃 |
③将实验②中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为a g. | / |
④分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入a g氧化铁粉末,向D试管中加入a g二氧化锰粉末,观察现象. | / |
(1)A中产生的气体是 ;B试管中的现象 .
(2)实验②、③证明:氧化铁的 和 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(3)写出氧化铁催化过氧化氢分解的文字表达式 .
(4)实验设计④的目的是 ,若实验④观察到D试管中产生气泡的速率更快,由此你可以得到的结论是 .