题目内容
探究金属性质时,将锌粒放入硫酸铜溶液中,锌粒表面有紫红色物质析出,还有无色无味气体产生的“异常”现象。推测该气体可能是
| A.氢气 | B.二氧化硫 | C.二氧化碳 | D.一氧化碳 |
A
解析试题分析:根据质量守恒定律反应前后原子的种类和数量不变,可以排除CD,依据置换反应的特点硫酸根要与金属锌结合,所以产生的气体可能是生成硫酸铜是剩余的硫酸与金属锌反应得到的氢气,故答案选择A
考点:质量守恒定律及置换反应

练习册系列答案
相关题目
下列符号中,表示2个氢分子的是
| A.H2 | B.2H | C.2H2 | D.2H+ |
下列化学方程式书写正确的是( )
A.Fe+O2 Fe3O4 Fe3O4 | B.2H2O=2H2+O2 |
C.Mg+O2 MgO2 MgO2 | D.2NaOH+SO3=Na2SO4+H2O |
发射“嫦娥三号”的长三甲火箭燃料是偏二甲肼(X),助燃剂是四氧化二氮(N2O4),反应的化学方程式为X+2N2O4=3N2+2CO2+4H2O,则X的化学式为
| A.H2 | B.CH4 | C.C2H8N | D.C2H8N2 |
下列物质的化学式书写正确的是
| A.碳酸钠NaCO3 | B.氢氧化钠Na(OH)2 |
| C.氧化铁FeO | D.硫酸H2SO4 |
如图为元素X的某粒子的结构示意图,下列说法正确的是( )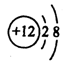
| A.该粒子可用符号“Mg+2”表示 | B.该粒子不带电 |
| C.X元素的核电荷数为10 | D.X与Cl形成的化合物为XCl2 |
潜水艇中可用过氧化钠制取氧气:2Na2O2+2CO2=2Na2CO3+O2,正确的说法是
| A.1mol Na2O2的质量为78g |
| B.1mol Na2O2含有1mol氧分子 |
| C.0.5mol Na2O2含有6.02×1023个原子 |
| D.反应前后氧元素的存在形态未发生改变 |
