题目内容
(2012?怀柔区一模)溶液在生活和生产中有着广泛的应用.某兴趣小组为了研究物质的溶解,做了如下所述的实验:
实验(1)
上述实验中可得到溶液的是
实验(2)
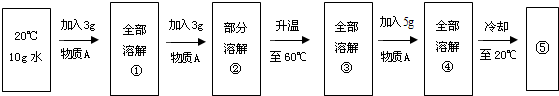
小资料:氯化钠和硝酸钾的溶解度数值:
物质A是
实验(1)
 |
 |
 |
| ①10克水中加入2克 碳酸钙 |
②10克水中加入2克 氯化钠 |
③10克汽油中加入2克氯化钠 |
②
②
(填序号),该溶液中的溶质是氯化钠
氯化钠
;①和②对比可得出影响物质溶解性的因素是溶质的性质
溶质的性质
;②和③对比可得出影响物质溶解性的因素是溶剂的性质
溶剂的性质
.实验(2)

小资料:氯化钠和硝酸钾的溶解度数值:
| 项目 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
| NaCl | 35.8g | 36.0g | 36.3g | 36.6g | 37.0g | 37.3g | 37.8g |
| KNO3 | 20.9g | 31.6g | 45.8g | 63.9g | 85.5g | 110g | 138g |
硝酸钾
硝酸钾
(填“氯化钠”或“硝酸钾”);上述实验过程中所得溶液达到饱和的是②④⑤
②④⑤
(填数字序号,下同);溶质质量分数最大的是④
④
.分析:实验(1)溶液的基本特征是均一性和稳定性;只有被分散的物质在另一种物质中是可溶的,二者混合后才会形成溶液;并由题中所给信息分析影响物质溶解性的因素;
实验(2)根据表中氯化钠和硝酸钾不同温度下的溶解度分析解答;以及饱和溶液与不饱和溶液的转化、硝酸钾的溶解度与溶质的质量分数的计算进行分析解答.
实验(2)根据表中氯化钠和硝酸钾不同温度下的溶解度分析解答;以及饱和溶液与不饱和溶液的转化、硝酸钾的溶解度与溶质的质量分数的计算进行分析解答.
解答:解:实验(1):三种物质中氯化钠能溶于水,碳酸钙不溶于水,氯化钠不溶于汽油,所以能形成溶液的是氯化钠加入水中形成的混合物,溶质是氯化钠;①和②对比可得出影响物质溶解性的因素是溶质的性质;②和③对比可得出影响物质溶解性的因素是溶剂的性质;
故答案为:②;氯化钠;溶质的性质;溶剂的性质;
实验(2):由题意可知10g水在60℃是能完全溶解6gA物质,而氯化钠在60℃时的溶解度为37.3g,硝酸钾的溶解度为110g,10g水最多溶解3.73g氯化钠,所以A物质不是氢化钠,是硝酸钾;
一定温度下溶液中有固体剩余就是饱和溶液,在20℃时10g水中最多溶解3.16g硝酸钾,而在60℃时10g水最多溶解硝酸钾11g,所以④也是饱和溶液;该转化过程中溶剂的质量未变,根据溶质的质量分数=
×100%可知,溶质的质量越大,溶质的质量分数越大,而④溶解的硝酸钾最多,故饱和溶液为“②④⑤”溶质质量分数最大的是④;
故答案为:硝酸钾;②④⑤;④.
故答案为:②;氯化钠;溶质的性质;溶剂的性质;
实验(2):由题意可知10g水在60℃是能完全溶解6gA物质,而氯化钠在60℃时的溶解度为37.3g,硝酸钾的溶解度为110g,10g水最多溶解3.73g氯化钠,所以A物质不是氢化钠,是硝酸钾;
一定温度下溶液中有固体剩余就是饱和溶液,在20℃时10g水中最多溶解3.16g硝酸钾,而在60℃时10g水最多溶解硝酸钾11g,所以④也是饱和溶液;该转化过程中溶剂的质量未变,根据溶质的质量分数=
| 溶质的质量 |
| 溶液的质量 |
故答案为:硝酸钾;②④⑤;④.
点评:掌握溶液的本质特征、各种物质的水溶性、明确溶质、溶剂的划分,会根据表中数据据解决问题,会判断某溶液是否饱和是解决此题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (2012?怀柔区一模)往如图所示的烧杯中加入一种物质,轻轻搅拌后,粘在烧杯底部的塑料片脱落,加入的物质不可能是( )
(2012?怀柔区一模)往如图所示的烧杯中加入一种物质,轻轻搅拌后,粘在烧杯底部的塑料片脱落,加入的物质不可能是( )