题目内容
长久使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除水垢.某学校化学课外兴趣小组的同学通过实验测定水垢中碳酸钙的含量,将过量的稀盐酸加到200g水垢中,同时测量3分钟内产生CO2的质量结果如下表:
计算水垢中碳酸钙质量分数.
| 时间/s | 30 | 50 | 90 | 150 | 180 |
| CO2质量/g | 30 | 50 | 60 | 66 | 66 |
碳酸钙能与盐酸反应生成二氧化碳,而氢氧化镁与盐酸反应不生成二氧化碳,当气体质量不再改变,说明碳酸钙已经反应完全,由表中的数据可知这些水垢完全反应生成二氧化碳的质量是66g;
设生成66g CO2需CaCO3的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 66g
=
x=150g
水垢中碳酸钙质量分数为:
×100%=75%
答:水垢中碳酸钙的质量为75%;
设生成66g CO2需CaCO3的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 66g
| 100 |
| x |
| 44 |
| 66g |
x=150g
水垢中碳酸钙质量分数为:
| 150g |
| 200g |
答:水垢中碳酸钙的质量为75%;

练习册系列答案
相关题目
长久使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除水垢.某学校化学课外兴趣小组的同学通过实验测定水垢中的碳酸钙的含量,将足量的稀盐酸加入到200g水垢中,同时测量3min内产生气体的质量,结果如下表:
试回答下列问题:
(1)表中有一个测量结果有较大的误差,这一点所对应的时间是 s.
(2)请在如图的坐标系上,以反应时间为横轴,以产生气体的质量为纵轴,画出能够表明产生气体的质量,随反应时间变化规律.
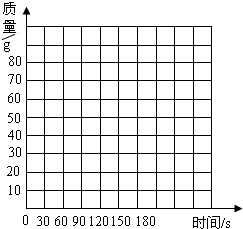
(3)计算该200g水垢中所含碳酸钙的质量及其质量分数.
| 时间/s | 0 | 30 | 50 | 90 | 120 | 150 | 180 |
| 质量/g | 0 | 30 | 50 | 60 | 80 | 66 | 66 |
(1)表中有一个测量结果有较大的误差,这一点所对应的时间是
(2)请在如图的坐标系上,以反应时间为横轴,以产生气体的质量为纵轴,画出能够表明产生气体的质量,随反应时间变化规律.

(3)计算该200g水垢中所含碳酸钙的质量及其质量分数.
长久使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除水垢.某学校化学课外兴趣小组的同学通过实验测定水垢中的碳酸钙的含量,将足量的稀盐酸加入到200g水垢中,同时测量3min内产生气体的质量,结果如下表:
| 时间/s | 0 | 30 | 50 | 90 | 120 | 150 | 180 |
| 质量/g | 0 | 30 | 50 | 60 | 80 | 66 | 66 |
(1)表中有一个测量结果有较大的误差,这一点所对应的时间是________s.
(2)请在如图的坐标系上,以反应时间为横轴,以产生气体的质量为纵轴,画出能够表明产生气体的质量,随反应时间变化规律.

(3)计算该200g水垢中所含碳酸钙的质量及其质量分数.
长久使用的热水壶底部有一层水垢,主要成分是CaCO3和Mg(OH)2。某学校化学研究性学习小组的同学通过实验测定水垢中CaCO3的含量:取200g水垢,加入过量的稀盐酸,同时测量5分钟内生成CO2的质量,结果如下表:
| 时间/分钟 | 1 | 2 | 3 | 4 | 5 |
| 质量/g | 30 | 50 | 60 | 66 | 66 |
试回答下列问题:
(1)4分钟后,水垢中CaCO3是否反应完全?
(2)该水垢中CaCO3的质量分数是多少?