题目内容
为测定某赤铁矿石中氧化铁的质量分数,小龙和他的同学用足量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,该溶液总质量与反应时间的变化关系如图.(1)上述反应产生二氧化碳的质量为______g;
(2)计算该赤铁矿石中氧化铁的质量分数.

(2)根据二氧化碳的已知量,设出未知量三氧化二铁,利用化学方程式3CO+Fe2O3
 2Fe+3CO2,列比例式,即可求出三氧化二铁的质量,然后根据氧化铁的质量分数;
2Fe+3CO2,列比例式,即可求出三氧化二铁的质量,然后根据氧化铁的质量分数;解答:解:(1)二氧化碳能与氢氧化钠反应生成碳酸钠和水,故溶液的增重值即为二氧化碳的质量,由图象知,反应产生二氧化碳的质量为106.6-100.0=6.6g;
(2)设赤铁矿石中氧化铁的质量为x,
3CO+Fe2O3
 2Fe+3CO2
2Fe+3CO2160 3×44
x 6.6g

解得x=8g
样品中氧化铁的质量分数为:
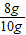 ×100%=80%
×100%=80%故答案为:(1)6.6;(2)答:该样品中氧化铁的质量分数为80%
点评:分析图表中数据时,要关注造成数据发生变化的原因,分析数据不再改变时所说明的问题,从而发现隐含条件.

某同学为测定10g某赤铁矿石中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3 2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题:
2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题:
得到如下数据:
| 装置 | B | C |
| 反应前质量 | 84.3g | 294.1g |
| 反应后质量 | 81.9g | 296.8g |
(1)请计算该赤铁矿石样品中氧化铁的质量分数。(写出计算过程)
(2)该实验还可测定组成水中各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为_______________________________________________(只列式,不计算);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会__________(选填“偏大”、“偏小” 或“不变”)。
某同学为测定10g某赤铁矿石中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3 2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题:
2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题:
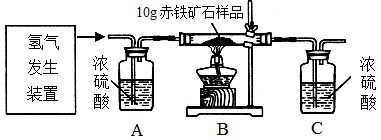
得到如下数据:
|
装置 |
B |
C |
|
反应前质量 |
84.3g |
294.1g |
|
反应后质量 |
81.9g |
296.8g |
(1)请计算该赤铁矿石样品中氧化铁的质量分数。(写出计算过程)
(2)该实验还可测定组成水中各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为_______________________________________________(只列式,不计算);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会__________(选填“偏大”、“偏小” 或“不变”)。
某同学为测定10g某赤铁矿石中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了下图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3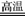 2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题:
2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收)。请回答有关问题:
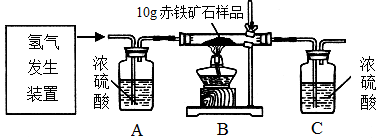
得到如下数据:
| 装置 | B | C |
| 反应前质量 | 84.3g | 294.1g |
| 反应后质量 | 81.9g | 296.8g |
(1)请计算该赤铁矿石样品中氧化铁的质量分数。(写出计算过程)
(2)该实验还可测定组成水中各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为_______________________________________________(只列式,不计算);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会__________(选填“偏大”、“偏小” 或“不变”)。