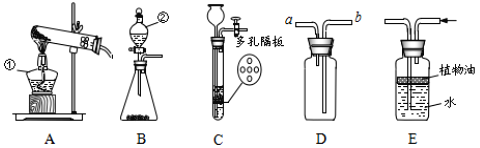
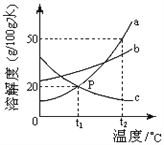
题目内容
【题目】轻质氧化镁(MgO)在橡胶工业上有重要用途。兴趣小组同学在实验室用工业炉渣废料(主要成分是MgO、CaO,含少量杂质SiO2)来制取轻质氧化镁,实验流程如下:
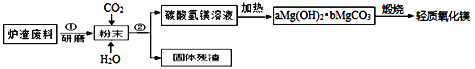
请根据流程图回答下列问题:
(1)步骤①研磨的目的是_________。
(2)操作②的名称是___________,所需要的玻璃仪器中玻璃棒的作用是_________。
【查阅资料】
① Mg(OH)2、MgCO3受热易分解,各生成对应的两种氧化物。
② Mg(OH)2的分解温度为340℃∽380℃,MgCO3的分解温度为520℃。
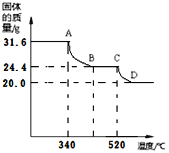
小组同学用热分析仪对aMg(OH)2bMgCO3固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如图,请根据图示回答下列问题:
(3)写出A B、C D段发生反应的化学方程式:
AB段:_______________________________;
CD段:_______________________________;
(4)BC段固体为 _____________________;
(5)通过计算可得:a : b=______________。
【答案】 增加接触面积,使其充分反应 过滤 引流 Mg(OH )2![]() MgO + H2O MgCO3
MgO + H2O MgCO3![]() MgO + CO2↑ MgO、MgCO3 4 :1
MgO + CO2↑ MgO、MgCO3 4 :1
【解析】(1)工业炉渣废料磨碎的目的是增加接触面积,使其充分反应;
(2)操作②的将固体和液体分开,所以操作为过滤,过滤时玻璃棒的作用是引流;
(3)由于Mg(OH)2的分解温度为340℃∽380℃,MgCO3的分解温度为520℃。
AB段由340℃开始反应,表示氢氧化镁在加热的条件下生成氧化镁和水,化学方程式为:Mg(OH )2![]() MgO + H2O;
MgO + H2O;
CD段由520℃开始反应,表示碳酸镁在加热的条件下生成氧化镁和二氧化碳,化学方程式为:MgCO3![]() MgO + CO2↑;
MgO + CO2↑;
(4)AB段由340℃开始反应,表示氢氧化镁在加热的条件下生成氧化镁和水, BC段反应完全,碳酸镁还没有分解,所以固体为:MgO、MgCO3;
(5)AB段是氢氧化镁在分解,固体质量减少31.6g-24.4g=7.2g,CD段是碳酸镁在分解,固体质量减少24.4g-20.0g=4.4g,Mg(OH )2![]() MgO + H2O;MgCO3
MgO + H2O;MgCO3![]() MgO + CO2↑;从方程式可以看出一个氢氧化镁分子分解会生成一个水分子,一个碳酸镁分子分解会产生一个二氧化碳分子,而AB段的氢氧化镁减少了7.2克水,CD段的碳酸镁分解减少了4.4克二氧化碳,减少了水分子与减少了二氧化碳分子的个数比为:
MgO + CO2↑;从方程式可以看出一个氢氧化镁分子分解会生成一个水分子,一个碳酸镁分子分解会产生一个二氧化碳分子,而AB段的氢氧化镁减少了7.2克水,CD段的碳酸镁分解减少了4.4克二氧化碳,减少了水分子与减少了二氧化碳分子的个数比为: ![]() =4:1,所以a:b=4:1。
=4:1,所以a:b=4:1。