题目内容
【题目】在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题: 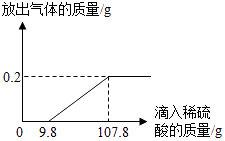
(1)产生氢气的质量为g;
(2)所滴加的稀硫酸中溶质的质量分数.
【答案】
(1)0.2
(2)解:设生成0.2g氢气需要硫酸的质量为x,
2Al+ | 3H2SO4=Al2(SO4)3+ | 3H2↑ |
294 | 6 | |
x | 0.2g |
则 ![]() ,解之得x=9.8g.
,解之得x=9.8g.
此时与生成氢气有关的硫酸溶液的质量为107.8g﹣9.8g=98g.
则稀硫中溶质的质量分数为: ![]() ×100%═10%
×100%═10%
答:所滴加的稀硫酸中溶质的质量分数10%
【解析】解:(1)根据铝箔和稀硫酸反应化学方程式,结合题干中的右图所示知道产生氢气的质量是0.2g;所以答案是:(1)0.2;(2)10%.
【考点精析】本题主要考查了根据化学反应方程式的计算的相关知识点,需要掌握各物质间质量比=系数×相对分子质量之比才能正确解答此题.

练习册系列答案
相关题目