题目内容
【题目】某无色气体可能含有CO2、CO、H2中的一种或几种,依次进行以下实验(假设每步反应均完全进行);①通过赤热的炭层后,恢复到原状态,气体体积不变;②通过灼热的CuO时,固体变成红色;③通过白色CuS04粉末时,粉末变成蓝色晶体;④通人澄清石灰水中,石灰水变浑浊。下列判断正确的是( )
A. 原混合气体中一定含有CO2、CO、H2
B. 原混合气体中一定没有CO2,一定含有H2和CO
C. 原混合气体中一定含H2和CO2,可能含CO
D. 原混合气体中一定含有CO2,可能含有CO、H2
【答案】B
【解析】
2分子的气态二氧化碳会和固态的碳反应生成1分子气态一氧化碳,化学方程式为CO2+C![]() 2CO,现通过赤热的炭层后,恢复到原状态,气体体积不变,说明没有二氧化碳;通过灼热的CuO时,固体变成红色,说明含有一氧化碳或氢气中的一种;通过白色CuS04粉末时,粉末变成蓝色晶体,说明上一步骤生成了水,即氢气和氧化铜反应生成铜单质和水,即原混合气体中含有氢气。由石灰水变浑浊说明混合气体中含有二氧化碳,但这些二氧化碳不是原气体中的,而是由于一氧化碳还原氧化铜生成二氧化碳,故原气体中一定含有一氧化碳。综上所述,原混合气体中一定没有CO2,一定含有H2和CO。故选B。
2CO,现通过赤热的炭层后,恢复到原状态,气体体积不变,说明没有二氧化碳;通过灼热的CuO时,固体变成红色,说明含有一氧化碳或氢气中的一种;通过白色CuS04粉末时,粉末变成蓝色晶体,说明上一步骤生成了水,即氢气和氧化铜反应生成铜单质和水,即原混合气体中含有氢气。由石灰水变浑浊说明混合气体中含有二氧化碳,但这些二氧化碳不是原气体中的,而是由于一氧化碳还原氧化铜生成二氧化碳,故原气体中一定含有一氧化碳。综上所述,原混合气体中一定没有CO2,一定含有H2和CO。故选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
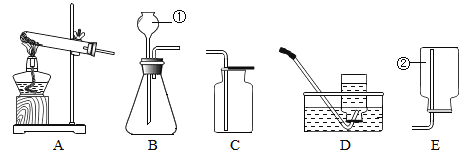
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
选项 | A | B | C | D |
实验装置 |
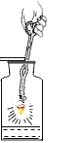
硫在氧气中燃烧 |
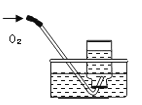
测定空气中氧气含量 |
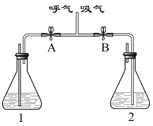
铁丝在氧气中燃烧 |
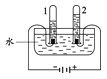
排水法收集氢气 |
解释 | 集气瓶中的水吸收放出的热量 | 量筒中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落熔融物,防止集气瓶炸裂 | 集气瓶中的水:用水将机器瓶内的空气排净后,便于观察O2何时收集满 |
A. A B. B C. C D. D