��Ŀ����
�������ƣ�NaN3�����㷺Ӧ����������ȫ���ң�ij��ȤС���ԱС����С������������̽����
��1������������Һ̬����Ӧ��NaNH2���ٽ�NaNH2��N2O��Ӧ������NaN3��NaOH������X���÷�Ӧ�Ļ�ѧ����ʽΪ2NaNH2+N2O=NaN3+NaOH+X��ʵ���Ҽ���X����ʹ�õ���ֽ�� ��
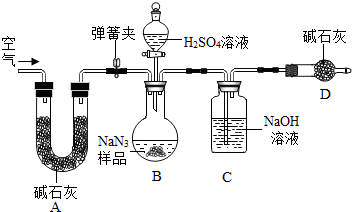
��2��Na2CO3���������ⶨ����ҵ��NaN3�г�����������Na2CO3��Ϊ�ⶨ��Ʒ��Na2CO3����������С�������ͼװ�ã���֪H2SO4��Һ��NaN3��Ӧ���������壩��ʵ�鲽�裺
�پ�ȷ������Ʒ����m1Ϊ7.12g�����װ��������
�ڴ��ɼУ��������������װ��C������Ϊm2
�۹رյ��ɼУ���Һ©������
�ܷ�Ӧ�������ٴγ���װ��CΪm3
С�쿴��С����ʵ����ƺ���ΪС����ʵ����ܻ���������������� ��
��3����С��������£�С����ʵ�鲽��۵ĺ������һ���������ò����� ��
��4������ȷ��ʵ������£����װ��C����Ϊ0.22g����ҵ��NaN3��Na2CO3����������Ϊ ��
��5����ҵ��NaN3�к���Na2CO3�Ŀ���ԭ���ǣ��û�ѧ����ʽ��ʾ�� ��
��6��װ��D�������� ��

��1������������Һ̬����Ӧ��NaNH2���ٽ�NaNH2��N2O��Ӧ������NaN3��NaOH������X���÷�Ӧ�Ļ�ѧ����ʽΪ2NaNH2+N2O=NaN3+NaOH+X��ʵ���Ҽ���X����ʹ�õ���ֽ��
��2��Na2CO3���������ⶨ����ҵ��NaN3�г�����������Na2CO3��Ϊ�ⶨ��Ʒ��Na2CO3����������С�������ͼװ�ã���֪H2SO4��Һ��NaN3��Ӧ���������壩��ʵ�鲽�裺
�پ�ȷ������Ʒ����m1Ϊ7.12g�����װ��������
�ڴ��ɼУ��������������װ��C������Ϊm2
�۹رյ��ɼУ���Һ©������
�ܷ�Ӧ�������ٴγ���װ��CΪm3
С�쿴��С����ʵ����ƺ���ΪС����ʵ����ܻ����������������
��3����С��������£�С����ʵ�鲽��۵ĺ������һ���������ò�����
��4������ȷ��ʵ������£����װ��C����Ϊ0.22g����ҵ��NaN3��Na2CO3����������Ϊ
��5����ҵ��NaN3�к���Na2CO3�Ŀ���ԭ���ǣ��û�ѧ����ʽ��ʾ��
��6��װ��D��������
���㣺ʵ��̽�����ʵ���ɳɷ��Լ�����,��������ļ�������ӷ���,�εĻ�ѧ����,�����غ㶨�ɼ���Ӧ��,��д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ,���ݻ�ѧ��Ӧ����ʽ�ļ���
ר�⣺��ѧ̽��
����������Ŀ����Ϣ�������غ㶨�ɿ�֪����ѧ����ʽ2NaNH2+N2O=NaN3+NaOH+X�У�X�ǰ���������������ʪ��ĺ�ɫʯ����ֽ�����飻С�쿴��С����ʵ����ƺ���ΪС����ʵ����ܻ���������������ǣ������Ķ�����̼û��ȫ����Cװ���е�����������Һ���գ�һ���ֶ�����̼����Bװ���У�С����ʵ�鲽��۵ĺ������һ���������ò����ǣ����ɼУ�����������Ѷ�����̼ȫ���ϳ�������ȷ��ʵ������£����װ��C����Ϊ0.22g��˵�����ɶ�����̼2.2g�����ݶ�����̼��������̼���Ƶ������������ɣ���ҵ��NaN3�к���Na2CO3�Ŀ���ԭ���ǣ��������Ĺ������������������ƣ������еĶ�����̼������������Һ��Ӧ����̼���ƺ�ˮ����ƽ���ɣ�װ��D�������ǣ����տ����еĶ�����̼����ֹ������̼��Cװ�����գ�
����⣺��1����ѧ����ʽ2NaNH2+N2O=NaN3+NaOH+X�У�X�ǰ���������������ʪ��ĺ�ɫʯ����ֽ�����飬�ʴ�Ϊ��ʪ��ĺ�ɫʯ����ֽ�����飻
��2��С�쿴��С����ʵ����ƺ���ΪС����ʵ����ܻ���������������ǣ������Ķ�����̼û��ȫ����Cװ���е�����������Һ���գ�һ���ֶ�����̼����Bװ���У��ʴ�Ϊ�������Ķ�����̼û��ȫ����Cװ���е�����������Һ���գ�һ���ֶ�����̼����B�У�
��3��С����ʵ�鲽��۵ĺ������һ���������ò����ǣ����ɼУ�����������Ѷ�����̼ȫ���ϳ����ʴ�Ϊ�����ɼУ����������
��4����Na2CO3������Ϊx��
Na2CO3+H2SO4=Na2SO4+H2O+CO2��
106 44
x 0.22g
=
x=0.53g��
��100%��7.4%��
�ʴ�Ϊ��7.4%
��5����ҵ��NaN3�к���Na2CO3�Ŀ���ԭ���ǣ��������Ĺ������������������ƣ������еĶ�����̼������������Һ��Ӧ����̼���ƺ�ˮ����ƽ���ɣ��ʴ�Ϊ��CO2+2NaOH=Na2CO3+H2O
��6��װ��D�������ǣ����տ����еĶ�����̼����ֹ������̼��Cװ�����գ��ʴ�Ϊ�����տ����еĶ�����̼����ֹ������̼��Cװ�����գ�
��2��С�쿴��С����ʵ����ƺ���ΪС����ʵ����ܻ���������������ǣ������Ķ�����̼û��ȫ����Cװ���е�����������Һ���գ�һ���ֶ�����̼����Bװ���У��ʴ�Ϊ�������Ķ�����̼û��ȫ����Cװ���е�����������Һ���գ�һ���ֶ�����̼����B�У�
��3��С����ʵ�鲽��۵ĺ������һ���������ò����ǣ����ɼУ�����������Ѷ�����̼ȫ���ϳ����ʴ�Ϊ�����ɼУ����������
��4����Na2CO3������Ϊx��
Na2CO3+H2SO4=Na2SO4+H2O+CO2��
106 44
x 0.22g
| 106 |
| 44 |
| x |
| 0.22g |
| 0.53g |
| 7.12g |
�ʴ�Ϊ��7.4%
��5����ҵ��NaN3�к���Na2CO3�Ŀ���ԭ���ǣ��������Ĺ������������������ƣ������еĶ�����̼������������Һ��Ӧ����̼���ƺ�ˮ����ƽ���ɣ��ʴ�Ϊ��CO2+2NaOH=Na2CO3+H2O
��6��װ��D�������ǣ����տ����еĶ�����̼����ֹ������̼��Cװ�����գ��ʴ�Ϊ�����տ����еĶ�����̼����ֹ������̼��Cװ�����գ�
������������ȿ�����ʵ�鲽�����ƣ��ֿ����˻�ѧ����ʽ����д���йصļ��㣬����ʵ����������ۣ��ۺ��ԱȽ�ǿ��ʵ��̽�����ǽ������п����ȵ�֮һ��������ʵ�鷽�����̵�̽����ʵ����ۺ�ʵ����ɵ�̽���ȣ�����ͨ��ʵ�����Ϻ�ʵ��������õ�����ȷ�Ľ��ۣ����ڽ�����̽����ͬѧ��Ҫ����������ۺ����գ�

��ϰ��ϵ�д�
 ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д� �����������ҵ�������������ϵ�д�
�����������ҵ�������������ϵ�д� ѧ���������ν��Ͼ���ѧ������ϵ�д�
ѧ���������ν��Ͼ���ѧ������ϵ�д�
�����Ŀ
����ҩƷ�������Ӽ�ȡ���ǣ�������
| A��ʳ�η�ĩ |
| B����״����ʯ |
| C��������ؿ��� |
| D���������̷�ĩ |
 ����ͼ��ʾ̽�������˶���ʵ���У�
����ͼ��ʾ̽�������˶���ʵ���У�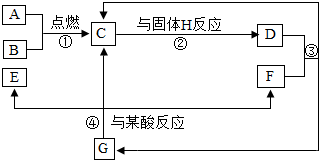 ���л�ѧ�м��ֳ�����������ͼ��ʾ��ת����ϵ������A��B������Ϊ���嵥�ʣ���Ӧ�ܳ�����ʵ������F���壬GΪ������ˮ�İ�ɫ���壮��ش��������⣺
���л�ѧ�м��ֳ�����������ͼ��ʾ��ת����ϵ������A��B������Ϊ���嵥�ʣ���Ӧ�ܳ�����ʵ������F���壬GΪ������ˮ�İ�ɫ���壮��ش��������⣺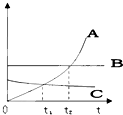 ��ͼ��A��B��C�������ʵ��ܽ�����ߣ����ͼ�ش�
��ͼ��A��B��C�������ʵ��ܽ�����ߣ����ͼ�ش�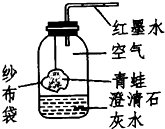 ijͬѧΪ�о�����ĺ������ã�����ͼ��ʾװ�ý���ʵ�飬ʵ������н��۲쵽������ʯ��ˮ
ijͬѧΪ�о�����ĺ������ã�����ͼ��ʾװ�ý���ʵ�飬ʵ������н��۲쵽������ʯ��ˮ