题目内容
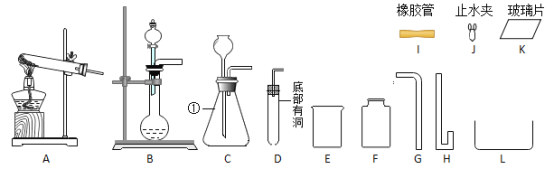
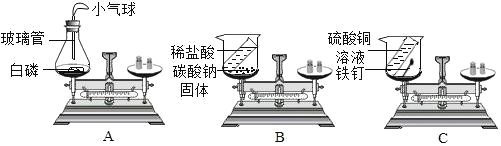
【题目】小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀硫酸和相关的仪器.
(1)根据现有的条件,你认为只能测出_____合金中铜的质量分数;
(2)为研究该合金的组成,某学习小组称取该样品10g,向其中逐滴加稀硫酸至刚好 不再产生气体为止.生成的气体与所用硫酸溶液的质量关系如图所示,请计算:
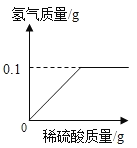
①生成的氢气的质量为_______g。
②样品中铜的质量分数是____?(写出计算过程)
【答案】Cu-Zn 0.1g 67.5%
【解析】
(1)在金属活动性顺序中,氢前的金属能与酸反应生成氢气,利用酸测定合金中铜的质量分数,则含有的另一种金属需在氢前,所以为:Cu-Zn;
(2) ①由图象可知,生成氢气的质量为0.1g,
②设合金中锌的质量为x,
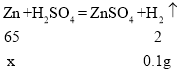
![]()
x=3.25g,
则合金中铜的质量为:10g-3.25g=6.75g,
因此,铜的质量分数为![]() ;
;
答:铜的质量分数为67.5%。

练习册系列答案
相关题目