题目内容
化学老师交给某学校研究性学习小组一个任务:测定实验室里一瓶久置的NaOH固体是否变质.该小组的同学进行了如下实验探究:
提出问题:猜想I:没变质,全部是NaOH;
猜想II:部分变质,________;
猜想Ⅲ:完全变质,全部是Na2CO3.
查阅资料:部分溶液在常温下的pH如下:
| 盐溶液 | NaCl | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品10.0g溶于100ml,水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有 ________(填化学式). |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH. | pH=11 | 说明久置固体中,还一定含有 ________ (填化学式). |
实验结论:通过实验,说明上述猜想中________是正确的.
拓展:该小组同学为测定出该NaOH固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为4.0g,则原样品中NaOH的质量分数为________ (保留一位小数).
反思:久置的氢氧化钠变质的原因是________(用化学方程式表示).
NaOH和Na2CO3. Na2CO3 NaOH 烧杯 让碳酸钠全部参加反应 猜想Ⅱ 78.5% 2NaOH+CO2═Na2CO3+H2O
分析:猜想Ⅱ:部分变质,说明一部分氢氧化钠发生了反应,氢氧化钠和空气中的二氧化碳生成碳酸钠和水.设计方案并进行实验:碳酸钠和氯化钡生成碳酸钡沉淀和氯化钠,反应后溶液中溶质有氯化钠和氯化钡(剩余).根据图表可知,氯化钠溶液和氯化钡溶液的pH都等于7,所以pH=11说明溶液中还有氢氧化钠.
实验结论:白色沉淀说明样品中有碳酸钠,pH=11说明样品中有氢氧化钠.
拓展:由沉淀的质量可以计算出碳酸钠的质量,然后求NaOH的质量分数.
反思:根据质量守恒定律可知.
解答:猜想Ⅱ:部分变质,说明一部分氢氧化钠发生了反应,氢氧化钠和空气中的二氧化碳生成碳酸钠和水,故答案为:NaOH和Na2CO3.
设计方案并进行实验:①碳酸钠和氯化钡生成碳酸钡沉淀和氯化钠,因此白色沉淀说明样品中含有碳酸钠.反应后溶液中溶质肯定有氯化钠和氯化钡(剩余),根据图表可知,氯化钠溶液和氯化钡溶液的pH都等于7,所以pH=11说明溶液中还有氢氧化钠.碳酸钠溶液的pH也大于7,所以根据pH=11就无法断定是否是氢氧化钠.故答案为:Na2CO3 ;
NaOH;烧杯;让碳酸钠全部参加反应.
实验结论:白色沉淀说明样品中有碳酸钠,pH=11说明样品中有氢氧化钠,故答案为:猜想Ⅱ.
拓展:根据题目信息可知,沉淀(碳酸钡)的质量是4克,设碳酸钠的质量是X.
Na2CO3+BaCl2═BaCO3↓+2NaCl
106 197
X 4克
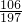 ═
═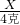
得:X=2.15克
∴样品中氢氧化钠的质量=10克-2.15克=7.85克,则原样品中NaOH的质量分数= ×100%═78.5%,故答案为:78.5%.
×100%═78.5%,故答案为:78.5%.
反思:根据质量守恒定律可知,空气中二氧化碳参加反应,故答案为:2NaOH+CO2═Na2CO3+H2O.
点评:掌握分析物质组成的方法,鉴别物质一般要求是现象明显,比如:沉淀、气体.
分析:猜想Ⅱ:部分变质,说明一部分氢氧化钠发生了反应,氢氧化钠和空气中的二氧化碳生成碳酸钠和水.设计方案并进行实验:碳酸钠和氯化钡生成碳酸钡沉淀和氯化钠,反应后溶液中溶质有氯化钠和氯化钡(剩余).根据图表可知,氯化钠溶液和氯化钡溶液的pH都等于7,所以pH=11说明溶液中还有氢氧化钠.
实验结论:白色沉淀说明样品中有碳酸钠,pH=11说明样品中有氢氧化钠.
拓展:由沉淀的质量可以计算出碳酸钠的质量,然后求NaOH的质量分数.
反思:根据质量守恒定律可知.
解答:猜想Ⅱ:部分变质,说明一部分氢氧化钠发生了反应,氢氧化钠和空气中的二氧化碳生成碳酸钠和水,故答案为:NaOH和Na2CO3.
设计方案并进行实验:①碳酸钠和氯化钡生成碳酸钡沉淀和氯化钠,因此白色沉淀说明样品中含有碳酸钠.反应后溶液中溶质肯定有氯化钠和氯化钡(剩余),根据图表可知,氯化钠溶液和氯化钡溶液的pH都等于7,所以pH=11说明溶液中还有氢氧化钠.碳酸钠溶液的pH也大于7,所以根据pH=11就无法断定是否是氢氧化钠.故答案为:Na2CO3 ;
NaOH;烧杯;让碳酸钠全部参加反应.
实验结论:白色沉淀说明样品中有碳酸钠,pH=11说明样品中有氢氧化钠,故答案为:猜想Ⅱ.
拓展:根据题目信息可知,沉淀(碳酸钡)的质量是4克,设碳酸钠的质量是X.
Na2CO3+BaCl2═BaCO3↓+2NaCl
106 197
X 4克
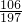 ═
═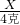
得:X=2.15克
∴样品中氢氧化钠的质量=10克-2.15克=7.85克,则原样品中NaOH的质量分数=
 ×100%═78.5%,故答案为:78.5%.
×100%═78.5%,故答案为:78.5%.反思:根据质量守恒定律可知,空气中二氧化碳参加反应,故答案为:2NaOH+CO2═Na2CO3+H2O.
点评:掌握分析物质组成的方法,鉴别物质一般要求是现象明显,比如:沉淀、气体.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
化学老师交给某学校研究性学习小组一个任务:测定实验室里一瓶久置的NaOH固体是否变质.该小组的同学进行了如下实验探究:
提出问题:猜想I:没变质,全部是NaOH;
猜想II:部分变质, ;
猜想Ⅲ:完全变质,全部是Na2CO3.
查阅资料:部分溶液在常温下的pH如下:
设计方案并进行实验:请你与他们一起共同完成,并回答所给问题.
上述步骤①中,称量氢氧化钠固体样品用到的玻璃仪器名称是 ,滴加过量BaCl2溶液的目的是
实验结论:通过实验,说明上述猜想中 是正确的.
拓展:该小组同学为测定出该NaOH固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为4.0g,则原样品中NaOH的质量分数为 (保留一位小数).
反思:久置的氢氧化钠变质的原因是 (用化学方程式表示).
提出问题:猜想I:没变质,全部是NaOH;
猜想II:部分变质,
猜想Ⅲ:完全变质,全部是Na2CO3.
查阅资料:部分溶液在常温下的pH如下:
| 盐溶液 | NaCl | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品10.0g溶于100ml,水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有 |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH. | pH=11 | 说明久置固体中,还一定含有 |
实验结论:通过实验,说明上述猜想中
拓展:该小组同学为测定出该NaOH固体的变质程度,继续将上述白色沉淀过滤、洗净、干燥,称得其质量为4.0g,则原样品中NaOH的质量分数为
反思:久置的氢氧化钠变质的原因是
化学老师交给某研究性学习小组一个任务:测定实验室里一瓶久置的NaOH固体是否变质.该小组的同学进行了如下实验探究:
【提出问题】
猜想I:没变质,全部是NaOH;
猜想II:部分变质,既含有NaOH又含有Na2CO3;
猜想Ⅲ:完全变质,全部是Na2CO3.
| 盐溶液 | NaCI | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品溶于水中,水配成溶液,向溶液中滴加 ①________至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有________(填化学式). |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有________ (填化学式). |
【实验结论】通过实验,说明上述猜想中________是正确的.
【反思】久置的氢氧化钠变质的原因是________(用化学方程式表示).
化学老师交给某研究性学习小组一个任务:测定实验室里一瓶久置的NaOH固体是否变质.该小组的同学进行了如下实验探究:
【提出问题】
猜想I:没变质,全部是NaOH;
猜想II:部分变质,既含有NaOH又含有Na2CO3;
猜想Ⅲ:完全变质,全部是Na2CO3.
【设计方案并进行实验】请你与他们一起共同完成,并回答所给问题.
滴加过量①溶液的目的是______
【实验结论】通过实验,说明上述猜想中______是正确的.
【反思】久置的氢氧化钠变质的原因是______(用化学方程式表示).
【提出问题】
猜想I:没变质,全部是NaOH;
猜想II:部分变质,既含有NaOH又含有Na2CO3;
猜想Ⅲ:完全变质,全部是Na2CO3.
| 盐溶液 | NaCI | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品溶于水中,水配成溶液,向溶液中滴加 ①______至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有______(填化学式). |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有______ (填化学式). |
【实验结论】通过实验,说明上述猜想中______是正确的.
【反思】久置的氢氧化钠变质的原因是______(用化学方程式表示).