题目内容
工业铁红主要成分是Fe2O3和Fe
(查阅资料])
①草酸晶体(H2C2O4·3H2O)在浓硫酸作用下受热分解,化学方程式为: 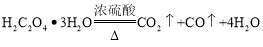
②碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。
(问题讨论)为了测定铁红中铁的质量分数,小凯和小滔进行了如下实验并称量了反应前铁红的质量,还称量了F在反应前后的质量。
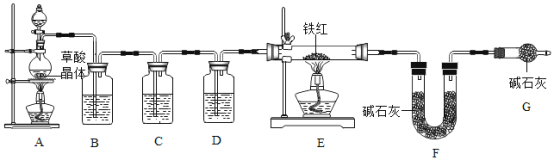
(1)实验前应先连接好仪器并______________________。
(2)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是______(填字母序号)。
a 浓硫酸 b 澄清的石灰水 c 氢氧化钠溶液
(3)写出E装置中所发生反应的化学方程式______________________。
(实验反思)(1)如果缺少G装置(不考虑其他因素),则测得样品中铁的质量分数会________(选填“偏小”“不变”“偏大”)。
(2)该实验装置的一个明显缺陷是________________________。
练习册系列答案
相关题目


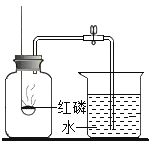
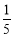 ,乙同学的广口瓶内水面上升明显大于瓶内空气体积的
,乙同学的广口瓶内水面上升明显大于瓶内空气体积的