题目内容
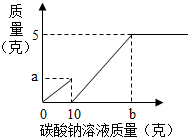 小芳在实验室用石灰石和稀盐酸制取了二氧化碳,并对实验产生的废液进行溶质成分鉴定:取废液上层清液50克,滴加质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克开始出现白色沉淀,继续滴加至沉淀不再产生,过滤,洗涤,干燥,称得沉淀质量为5克,并绘制了图象,如图:
小芳在实验室用石灰石和稀盐酸制取了二氧化碳,并对实验产生的废液进行溶质成分鉴定:取废液上层清液50克,滴加质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克开始出现白色沉淀,继续滴加至沉淀不再产生,过滤,洗涤,干燥,称得沉淀质量为5克,并绘制了图象,如图:
(1)图象中的a点数值______
(2)废液中含有的溶质是______(写化学式)
(3)通过计算说明,图象横坐标中b点表示的溶液的质量是多少?
解:(1)图象中的a点数值是二氧化碳的质量,设生成的二氧化碳的质量为x
Na2C03+2HCl=2NaCl+H2O+CO2↑
106 44
10g×26.5% x
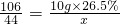 x=1.1g.
x=1.1g.
(2)取废液上层清液50克,滴加质量分数为26.5%的碳酸钠溶液,出现气泡,说明废液中含有盐酸;滴加至10克开始出现白色沉淀,说明废液中含有氯化钙;故废液是盐酸和氯化钙溶液的混合物,废液中含有的溶质是HCl、CaCl2.
(3)设与氯化钙反应的碳酸钠溶液中溶质质量为y,
CaCl2+Na2C03=2NaCl+CaC03↓
106 100
y 5g
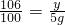 y=5.3g
y=5.3g
所需碳酸钠溶液质量是5.3g÷26.5%=20g
b点表示的溶液的质量为20g+10g=30g.
答:(1)1.1;(2)HCl、CaCl2;(3)图象横坐标中b点表示的溶液的质量是30g.
分析:石灰石和稀盐酸制取二氧化碳产生的废液中一定含有生成的氯化钙,可能含有盐酸;取废液上层清液50克,滴加质量分数为26.5%的碳酸钠溶液,出现气泡,说明废液中含有盐酸;滴加至10克开始出现白色沉淀,说明废液中含有氯化钙;故废液是盐酸和氯化钙溶液的混合物.
图象中的a点数值是产生的二氧化碳的质量,可以根据碳酸钠溶液的质量、溶质的质量分数求出;图象横坐标中的b点表示的碳酸钠溶液的质量,可以根据产生沉淀的质量为5g,由反应的化学方程式计算求出.
点评:本题有一定难度,掌握根据化学方程式的计算即可正确解答本题,细致地分析图象信息,明确反应原理是正确解答本题的前提和关键.
Na2C03+2HCl=2NaCl+H2O+CO2↑
106 44
10g×26.5% x
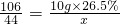 x=1.1g.
x=1.1g.(2)取废液上层清液50克,滴加质量分数为26.5%的碳酸钠溶液,出现气泡,说明废液中含有盐酸;滴加至10克开始出现白色沉淀,说明废液中含有氯化钙;故废液是盐酸和氯化钙溶液的混合物,废液中含有的溶质是HCl、CaCl2.
(3)设与氯化钙反应的碳酸钠溶液中溶质质量为y,
CaCl2+Na2C03=2NaCl+CaC03↓
106 100
y 5g
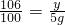 y=5.3g
y=5.3g所需碳酸钠溶液质量是5.3g÷26.5%=20g
b点表示的溶液的质量为20g+10g=30g.
答:(1)1.1;(2)HCl、CaCl2;(3)图象横坐标中b点表示的溶液的质量是30g.
分析:石灰石和稀盐酸制取二氧化碳产生的废液中一定含有生成的氯化钙,可能含有盐酸;取废液上层清液50克,滴加质量分数为26.5%的碳酸钠溶液,出现气泡,说明废液中含有盐酸;滴加至10克开始出现白色沉淀,说明废液中含有氯化钙;故废液是盐酸和氯化钙溶液的混合物.
图象中的a点数值是产生的二氧化碳的质量,可以根据碳酸钠溶液的质量、溶质的质量分数求出;图象横坐标中的b点表示的碳酸钠溶液的质量,可以根据产生沉淀的质量为5g,由反应的化学方程式计算求出.
点评:本题有一定难度,掌握根据化学方程式的计算即可正确解答本题,细致地分析图象信息,明确反应原理是正确解答本题的前提和关键.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目

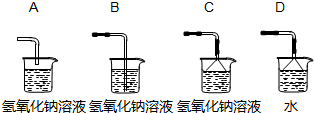


 小芳在实验室用石灰石和稀盐酸制取了二氧化碳,并对实验产生的废液进行溶质成分鉴定:取废液上层清液50克,滴加质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克开始出现白色沉淀,继续滴加至沉淀不再产生,过滤,洗涤,干燥,称得沉淀质量为5克,并绘制了图象,如图:
小芳在实验室用石灰石和稀盐酸制取了二氧化碳,并对实验产生的废液进行溶质成分鉴定:取废液上层清液50克,滴加质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克开始出现白色沉淀,继续滴加至沉淀不再产生,过滤,洗涤,干燥,称得沉淀质量为5克,并绘制了图象,如图: