题目内容
实验室中敞开盛有浓盐酸的试剂瓶,瓶口立即产生大量白雾;把盛有浓氨水的试剂瓶敞开,在瓶口却看不到白雾.同学们对氨气在空气中不能产生白雾的原因进行了如下探究:
[查阅资料]雾的形成条件有三:①有小液滴;②有空气;③小液滴在空气中分散必须十分密集,达到肉眼可见的程度.
[猜想]甲同学的猜想是:浓氨水的挥发性不强,瓶口附近空气中的氨气少,形成的氨水小液滴少,即小液滴分布不密集而不能产生雾.
乙同学的猜想是:氨气的扩散速率比氯化氢大,因此浓氨水挥发出来的氨气会快速向四周扩散,它与空气中水蒸气结合形成的氨水小液滴不能集中,即不可能形成雾.
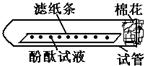
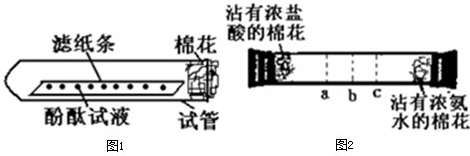
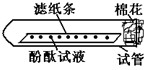
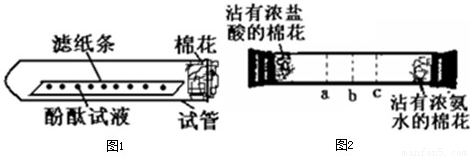
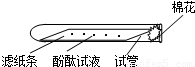
[实验论证]实验一:如下图所示,取一条长10cm、宽1cm的滤纸条,在滤纸条上每隔1、5cm-2cm处滴一小滴酚酞试液.滴好后把滤纸条放到试管里,在试管口塞上一小团棉花.然后用滴管吸取浓氨水,在试管口的棉花上滴10-15滴.
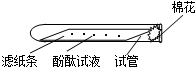
实验现象:________.
实验结论:浓氨水挥发出大量的氨气,且氨分子不断向周围扩散.所以甲同学的猜想不成立.
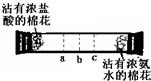
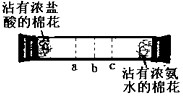
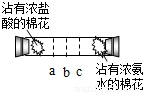
实验二:如下图所示,在一口径为2cm长50cm水平横放的中空玻璃管的两端,分别同时塞入沾有浓盐酸与浓氨水的棉花,立即用橡皮塞塞紧两端.
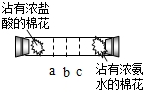
实验现象:数分钟后最有可能在试管中的________(选填a、b、c)处开始产生白烟.
白烟的成分是氯化铵(NH4Cl),形成白烟的原因是(用化学方程式表示):________,反应类型为________.
实验结论:氯化氢分子、氨分子都能扩散,且扩散速率氨气比氯化氢大.所以乙的猜想成立.
滤纸条由管口向管底依次变红 a处 NH3+HCl=NH4Cl 化合反应
分析:实验一是用来验证氨气的挥发性,氨气遇水呈碱性,能使无色酚酞变红色.
实验二是用来证明氨气比氯化氢扩散的快的,因为氨气的相对分子量小,故运动的要快,氨气与氯化氢能反应生成氯化铵,书写化学方程式时一定要把反应物和生成物的化学式写正确,本反应配平较简单,化学式前面的系数都是1,反应类型也比较明显,是两种物质生成一种物质.
解答:实验一中,因为氨气有挥发性,遇水呈碱性,能使无色酚酞变红色,故能看到滤纸条由管口向管底依次变红的现象.
实验二中,因为氨气比氯化氢气体运动的要快的多,故应该在a处看到白烟,白烟是氨气和氯化氢反应生成的氯化铵,反应的化学方程式为:NH3+HCl=NH4Cl,两种物质生成一种物质,属于化合反应.
故答案为:
实验一:滤纸条由管口向管底依次变红;
实验二:a处,NH3+HCl=NH4Cl,化合反应
点评:对于实验探究题,要大胆猜想,然后用科学的实验去验证猜想是否正确;通过本题可知分子的相对分子质量的大小决定分子运动速度的快慢,氨气分子要比氯化氢分子运动的快.
分析:实验一是用来验证氨气的挥发性,氨气遇水呈碱性,能使无色酚酞变红色.
实验二是用来证明氨气比氯化氢扩散的快的,因为氨气的相对分子量小,故运动的要快,氨气与氯化氢能反应生成氯化铵,书写化学方程式时一定要把反应物和生成物的化学式写正确,本反应配平较简单,化学式前面的系数都是1,反应类型也比较明显,是两种物质生成一种物质.
解答:实验一中,因为氨气有挥发性,遇水呈碱性,能使无色酚酞变红色,故能看到滤纸条由管口向管底依次变红的现象.
实验二中,因为氨气比氯化氢气体运动的要快的多,故应该在a处看到白烟,白烟是氨气和氯化氢反应生成的氯化铵,反应的化学方程式为:NH3+HCl=NH4Cl,两种物质生成一种物质,属于化合反应.
故答案为:
实验一:滤纸条由管口向管底依次变红;
实验二:a处,NH3+HCl=NH4Cl,化合反应
点评:对于实验探究题,要大胆猜想,然后用科学的实验去验证猜想是否正确;通过本题可知分子的相对分子质量的大小决定分子运动速度的快慢,氨气分子要比氯化氢分子运动的快.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目