题目内容
【题目】(1)小明在实验室做实验的时候,获得了两种溶液:氢氧化钠溶液和石灰水。
①如果他想验证某瓶气体样品中是否含有二氧化碳,他应该选用的是_________溶液,理由是________________。
②若想除去气体样品中的二氧化碳,他应该选用的是________溶液,理由是_________。
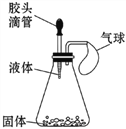
(2)如图所示,挤压胶头滴管,使其中的液体与瓶中固体接触,可使小气球鼓起来。请写出符合下列要求的化学方程式:
①分解反应___________________________________;
②化合反应___________________________________。
【答案】 氢氧化钙[或Ca(OH)2] CO2能使澄清石灰水变浑浊,有明显现象 氢氧化钠(或NaOH) NaOH易溶于水,吸收的CO2较多 2H2O2![]() 2H2O+O2↑ CaO+H2O====Ca(OH)2
2H2O+O2↑ CaO+H2O====Ca(OH)2
【解析】(1)①用澄清石灰水验证某瓶气体样品中含有二氧化碳;因为CO2能与澄清石灰水的主要成分Ca(OH)2反应生成CaCO3白色沉淀,而CO2与NaOH溶液反应无明显现象;
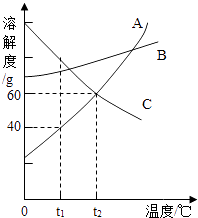
②用氢氧化钠溶液除去气体样品中的二氧化碳;因为氢氧化钠易溶于水,氢氧化钙微溶于水,两者分别溶于等量的水中,氢氧化钠溶液中溶质的质量分数比氢氧化钙溶液中溶质的质量分数大,所以氢氧化钠溶液吸收二氧化碳的效果更好;
(2)①分解反应生成气体,并且是常温下,过氧化氢分解时会放出氧气,使气球膨胀,滴管中是过氧化氢,锥形瓶底是二氧化锰,化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
②物质CaO与水反应放出大量的热,属于化合反应,则溶液的温度升高,使气体膨胀,气球变大,化学方程式为:CaO+H2O═Ca(OH)2。

【题目】某兴趣小组用KClO3和MnO2制取氧气,试管中固体的质量随时间变化的数据见下表.制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g.
加热时间\min | 0 | t1 | t2 | t3 |
固体质量\g | 28.0 | 23.2 | 18.4 | 18.4 |
(1)共制得氧气g
(2)计算所得氯化钾溶液的溶质质量分数是多少?