��Ŀ����
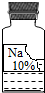 ��2012?Ϣ��һģ��ʵ��������һƿ���õ���ɫ��Һ���ܲ��������ȱ�ı�ǩ��ֻʣ�¡�Na���͡�10%����������ͼ��ʾ����Сǿ��С��ͬѧ�ܸ���Ȥ����������ɷֽ���̽����
��2012?Ϣ��һģ��ʵ��������һƿ���õ���ɫ��Һ���ܲ��������ȱ�ı�ǩ��ֻʣ�¡�Na���͡�10%����������ͼ��ʾ����Сǿ��С��ͬѧ�ܸ���Ȥ����������ɷֽ���̽������������⡿��ƿ�Լ�������ʲô��Һ�أ�
���������ۡ����������ǩ������жϣ���ƿ�Լ���������
A
A
��A���� B���� C����
���������ϡ�
����г������ƵĻ������У�NaCl��NaOH��Na2CO3��NaHCO3��
��Na2CO3��NaHCO3��ˮ��Һ���ʼ��ԣ�
�����£�20�棩ʱ���ⶨ�������ʵ��ܽ���������£�
| ���� | NaCl | NaOH | Na2CO3 | NaHCO3 |
| �ܽ��g | 36 | 109 | 215 | 9.6 |
NaHCO3
NaHCO3
�����������롿�ٿ�����NaCl���ڿ�����Na2CO3���ۿ�����
NaOH
NaOH
����ʵ��̽����
��1��Сǿ�ýྻ�IJ�����պȡ��Һ��pH��ֽ�ϣ����pH��7������ƿ�Լ���������
NaCl��Һ
NaCl��Һ
����2��СǿΪ�˼������Һ��NaOH��Һ����Na2CO3��Һ�����ֽ���������ʵ�飮
| ʵ�鲽�� | ʵ������ | ���ۼ���ѧ����ʽ |
| ��ȡ������Һ���Թ��У� �μ� ϡ���� ϡ���� �� |
������������ | ��Ӧ�Ļ�ѧ����ʽ�� Na2CO3+2HCl=2NaCl+H2O+CO2�� Na2CO3+2HCl=2NaCl+H2O+CO2�� �� |
| �ڰѲ���������ͨ�� �����ʯ��ˮ�У� |
�����ʯ��ˮ����� | �������ȷ����Ӧ�Ļ�ѧ����ʽ�� CO2+Ca��OH��2�TCaCO3��+H2O CO2+Ca��OH��2�TCaCO3��+H2O |
Ca��OH��2
Ca��OH��2
�����ۺϼ��㡿��ȡ�����Ȼ������ʵĴ�����Ʒ25g�����ձ��У������м���50gϡ���ᣬ����ǡ����ȫ��Ӧ����Ӧ����������ձ���ʣ�����ʵ�������Ϊ66.2g���������ձ�����������������ܽ���Բ��ƣ����Լ��㴿����Ʒ�������Ȼ��Ƶ�����������
���������������ۡ������ᡢ��ε�����ص㼰��ǩ�ɼ����֣��²����Һ�����������������ʵ���Һ��
���������ϡ�������Һ�������ܽ���뱥����Һ�����ʵ����������Ĺ�ϵ���ɳ����¸����ʵ��ܽ�ȼ�����Һ�����������������ж���Һ�Ŀ����ԣ�
���������롿������ʾ���ʵĿ����ԣ��Ը���Һ���в��룻
����Ʋ�ʵ�顿��1����������������Һ������Լ����ⶨ��Һ�����ȣ�����Һ�Ŀ��������жϣ�
��2������̼���ơ������������ʲ��켰�����ʵ���е������ж�����ȡ�ļ��������Լ��������ۣ�
����չ��Ӧ�á�����̼���ơ��������Ƶ����ʲ��죬��ѡһ���Լ�����������ʵļ���
���ۺϼ��㡿���ݷ�Ӧǰ���������������ɶ�����̼�����������ݻ�ѧ����ʽ����òμӷ�Ӧ��̼���Ƶ����������������Ʒ�����ʵ�����������
���������ϡ�������Һ�������ܽ���뱥����Һ�����ʵ����������Ĺ�ϵ���ɳ����¸����ʵ��ܽ�ȼ�����Һ�����������������ж���Һ�Ŀ����ԣ�
���������롿������ʾ���ʵĿ����ԣ��Ը���Һ���в��룻
����Ʋ�ʵ�顿��1����������������Һ������Լ����ⶨ��Һ�����ȣ�����Һ�Ŀ��������жϣ�
��2������̼���ơ������������ʲ��켰�����ʵ���е������ж�����ȡ�ļ��������Լ��������ۣ�
����չ��Ӧ�á�����̼���ơ��������Ƶ����ʲ��죬��ѡһ���Լ�����������ʵļ���
���ۺϼ��㡿���ݷ�Ӧǰ���������������ɶ�����̼�����������ݻ�ѧ����ʽ����òμӷ�Ӧ��̼���Ƶ����������������Ʒ�����ʵ�����������
����⣺���������ۡ������ǩ�ɼ�����Ϊ��Ԫ�أ����жϸ������ɽ���Ԫ�������ɣ���������������Ԫ�����������ɣ����жϸ����ʲ�����Ϊ�
���������ϡ����ݳ�����̼�����Ƶ���ҺΪ9.6g�����жϳ�����̼�����Ƶı�����Һ��������������=
��100%=8.8%����˿��жϸ���Һ������Ϊ̼��������Һ�����������ʽ������Ƶļ��㶼���Եõ�10%����Һ��
���������롿��̼�������⣬����Һ����Ϊ�Ȼ��ơ�̼���ƻ�����������Һ��
����Ʋ�ʵ�顿��1��Сǿ�ýྻ�IJ�����պȡ����Һ����pH��ֽ�ϣ����pH��7�����Ȼ�����Һ�����ԣ�pH����7���Բ��������Ȼ��ƣ�
��2���ٸ���̼�����������ᷴӦ�ų�������̼���������������ᷴӦ������������ˣ����ƶϼ���������ʱ��������Լ�Ϊϡ���ᣬ̼���������ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼��Ӧ�ķ���ʽΪ��Na2CO3+2HCl=2NaCl+H2O+CO2�����ڹ۲������ݿ�˵��������Ϊ̼���ƣ��Ѳ�������ͨ�����ʯ��ˮ��ʯ��ˮ�����ǣ���ɽ�һ��ȷ�������ʣ���Ӧ�Ļ�ѧ����ʽΪCO2+Ca��OH��2�TCaCO3��+H2O��
����չ��Ӧ�á�����������������̼���Ʒ�Ӧ���ɰ�ɫ̼��Ƴ����������������Ʋ��ܷ�Ӧ������������ʹ������������Һ����NaOH��Һ��Na2CO3��Һ��
���ۺϼ��㡿�⣺��μӷ�Ӧ��̼���Ƶ�����Ϊx
�������֪����Ӧ������������̼������Ϊ��25g+50g-66.2g=8.8g
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106 44
x 8.8g
=
x=21.2g
������Ʒ�����ʵ�������25g-21.2g=3.8g��
����Ʒ�������Ȼ��Ƶ���������Ϊ
��100%=15.2%��
�ʴ�Ϊ�����������ۡ�A��
���������ϡ�NaHCO3��
���������롿NaOH��
����Ʋ�ʵ�顿��1��NaCl��Һ��
����չ��Ӧ�á�Ca��OH��2��
���ۺϼ��㡿�𣺴�����Ʒ�������Ȼ��Ƶ���������Ϊ15.2%��
���������ϡ����ݳ�����̼�����Ƶ���ҺΪ9.6g�����жϳ�����̼�����Ƶı�����Һ��������������=
| 9.6g |
| 100g+9.6g |
���������롿��̼�������⣬����Һ����Ϊ�Ȼ��ơ�̼���ƻ�����������Һ��
����Ʋ�ʵ�顿��1��Сǿ�ýྻ�IJ�����պȡ����Һ����pH��ֽ�ϣ����pH��7�����Ȼ�����Һ�����ԣ�pH����7���Բ��������Ȼ��ƣ�
��2���ٸ���̼�����������ᷴӦ�ų�������̼���������������ᷴӦ������������ˣ����ƶϼ���������ʱ��������Լ�Ϊϡ���ᣬ̼���������ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼��Ӧ�ķ���ʽΪ��Na2CO3+2HCl=2NaCl+H2O+CO2�����ڹ۲������ݿ�˵��������Ϊ̼���ƣ��Ѳ�������ͨ�����ʯ��ˮ��ʯ��ˮ�����ǣ���ɽ�һ��ȷ�������ʣ���Ӧ�Ļ�ѧ����ʽΪCO2+Ca��OH��2�TCaCO3��+H2O��
����չ��Ӧ�á�����������������̼���Ʒ�Ӧ���ɰ�ɫ̼��Ƴ����������������Ʋ��ܷ�Ӧ������������ʹ������������Һ����NaOH��Һ��Na2CO3��Һ��
���ۺϼ��㡿�⣺��μӷ�Ӧ��̼���Ƶ�����Ϊx
�������֪����Ӧ������������̼������Ϊ��25g+50g-66.2g=8.8g
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106 44
x 8.8g
| 106 |
| x |
| 44 |
| 8.8g |
x=21.2g
������Ʒ�����ʵ�������25g-21.2g=3.8g��
����Ʒ�������Ȼ��Ƶ���������Ϊ
| 3.8g |
| 25g |
�ʴ�Ϊ�����������ۡ�A��
���������ϡ�NaHCO3��
���������롿NaOH��
����Ʋ�ʵ�顿��1��NaCl��Һ��
| ʵ�鲽�� | ʵ������ | ���ۼ���ѧ����ʽ |
| ϡ���� | Na2CO3+2HCl=2NaCl+H2O+CO2���� | |
| CO2+Ca��OH��2�TCaCO3��+H2O |
���ۺϼ��㡿�𣺴�����Ʒ�������Ȼ��Ƶ���������Ϊ15.2%��
�����������ۺ����������ʵ���ɡ����ʵ��ܽ��ԡ���Һ������Լ����ʵı仯���ɶ�δ֪���ʽ��м����������û�ѧ֪ʶ�������⡢��������������

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ