��Ŀ����
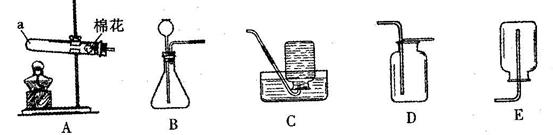
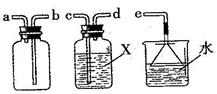
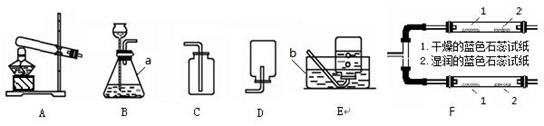
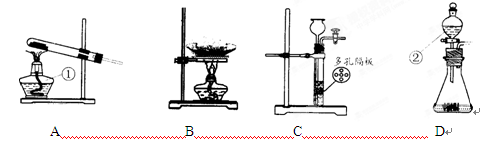
��7�֣���ͼΪʵ�����г����������Ʊ������������ʵ��IJ�����������ش��������⣺
 ��1�����Թ���������ҺΪԭ����ʵ�������Ʊ����ռ������������
��1�����Թ���������ҺΪԭ����ʵ�������Ʊ����ռ������������
����ѡ����������˳��Ϊ ����д���������ĸ����
����������ʱ����������Ӧ�Ļ�ѧ����ʽΪ ��
��2������һ������壬����Ҫ�ɷ�ΪCO����������ˮ�����������ܺ�������HCl���塣ijͬѧ���ø��﴿����CO���廹ԭ���������������� (���ʲ���Ӧ)������֤��Ӧ����������������ʡ�
����ѡ����������˳��Ϊ������������ ������ ������ ������ ������ ��
������D��������
���ڳ�ȥHCl��������в������Է�Ӧ�������û�ѧ����֤����������д����Ȼ������壬���AgNO3��Һ��Ca(OH)2��Һ��ϡ���������Լ���ѡ��һ������������������Һ�������飬����֤��������
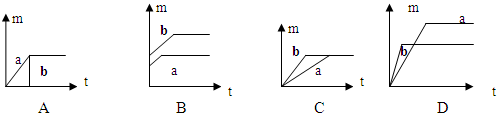
������10 g��Ʒ����Ӧ������ȫ��������D�����ʼ���2.4g������Ʒ���������Ĵ��� .
 ��1�����Թ���������ҺΪԭ����ʵ�������Ʊ����ռ������������
��1�����Թ���������ҺΪԭ����ʵ�������Ʊ����ռ����������������ѡ����������˳��Ϊ ����д���������ĸ����
����������ʱ����������Ӧ�Ļ�ѧ����ʽΪ ��
��2������һ������壬����Ҫ�ɷ�ΪCO����������ˮ�����������ܺ�������HCl���塣ijͬѧ���ø��﴿����CO���廹ԭ���������������� (���ʲ���Ӧ)������֤��Ӧ����������������ʡ�
����ѡ����������˳��Ϊ������������ ������ ������ ������ ������ ��
������D��������
���ڳ�ȥHCl��������в������Է�Ӧ�������û�ѧ����֤����������д����Ȼ������壬���AgNO3��Һ��Ca(OH)2��Һ��ϡ���������Լ���ѡ��һ������������������Һ�������飬����֤��������
������10 g��Ʒ����Ӧ������ȫ��������D�����ʼ���2.4g������Ʒ���������Ĵ��� .
��1����A��B��G
��2H2O2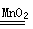 2H2O+ O2��
2H2O+ O2��
��2������ѡ����������˳��Ϊ������������F������B������D������E������C��
�ں�ɫ��ĩ���ɫ
��AgNO3��Һ ����Һ�г��ְ�ɫ����˵�����Ȼ����AgNO3+HCl==AgCl��+HNO3
��80%
��2H2O2
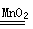 2H2O+ O2��
2H2O+ O2����2������ѡ����������˳��Ϊ������������F������B������D������E������C��
�ں�ɫ��ĩ���ɫ
��AgNO3��Һ ����Һ�г��ְ�ɫ����˵�����Ȼ����AgNO3+HCl==AgCl��+HNO3
��80%
��1���Թ���������ҺΪԭ���Ʊ�����ʱ������Ҫ���ȣ�Ũ���������ˮ�ԣ��������������ռ���������壻��2��һ����̼�л����Ȼ��������ˮ�������Ȼ�������������������Һ���գ�Ũ������Ը���һ����̼��һ����̼��ԭ�������������Ͷ�����̼��������̼��ʹ�����ʯ��ˮ����ǣ���ԭ���������β���л���ʣ���һ����̼��һ����̼�ж�������Ⱦ������Ӧ�õ�ȼ�ķ��������ȥ���۸�������������������Ȼ����������н��
�ܹ���ǰ�������仯�ǣ�43.7g-41.3g=2.4g��
��������������ΪX��
Fe2O3+3CO=2Fe+3CO2�� ���������仯
160 112 48
X 2.4g
160��48=X��2.4g
X=8g��
������������������8g /10g ��100%=80%��
�ܹ���ǰ�������仯�ǣ�43.7g-41.3g=2.4g��
��������������ΪX��
Fe2O3+3CO=2Fe+3CO2�� ���������仯
160 112 48
X 2.4g
160��48=X��2.4g
X=8g��
������������������8g /10g ��100%=80%��

��ϰ��ϵ�д�
 ������ϰ�ο����뵥Ԫ���ϵ�д�
������ϰ�ο����뵥Ԫ���ϵ�д� �����Ծ���ĩ���100��ϵ�д�
�����Ծ���ĩ���100��ϵ�д� ˫��ͬ������ѵ��ϵ�д�
˫��ͬ������ѵ��ϵ�д�
�����Ŀ

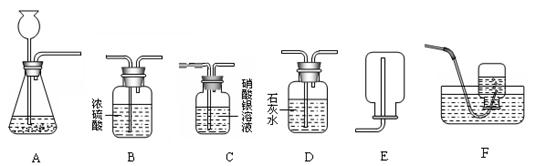 ��1���Խ���п��ϡ����Ϊԭ����ȡ���ռ������������������ʾ�������лӷ���������HCl���������������Һ���գ���
��1���Խ���п��ϡ����Ϊԭ����ȡ���ռ������������������ʾ�������лӷ���������HCl���������������Һ���գ���