题目内容
【题目】某化学兴趣小组用化学方法测定一种钢样品中铁的含量.同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中.在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如表:
反应时间 | t0 | t1 | t2 | t3 |
烧杯和药品质量/g | 25.7 | 25.6 | 25.5 | 25.5 |
(1)反应中产生氢气克,这种钢样品中铁的含量是多少?(精确到0.1%)
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢.假设残留在烧杯中的黑色固体全部是炭,则这种钢属于 .
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻.可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多.原因是 .
【答案】
(1)0.2g
(2)高碳钢
(3)钢中含碳量少,碳减少的质量远小于铁转化为氧化物增加的质量
【解析】解:(1)根据质量守恒,反应前后质量差即为氢气质量,生成氢气的质量=5.7g+10g+10g﹣25.5g=0.2g; 设5.7g钢样品中铁的质量为x
Fe+2HCl=FeCl2+ | H2↑ |
56 | 2 |
x | 0.2g |
![]()
解得,x=5.6g
则这种钢样品铁的含量为: ![]() ×100%≈98.2%;
×100%≈98.2%;
答:这种钢样品中铁的含量是98.2%;(2)这种钢样品中含碳量为:1﹣98.2%=1.8%,0.6%<1.8%<2%,故这种钢属于高碳钢;
故答案是:高碳钢(3)钢样灼烧时,钢样中的铁与氧气化合成铁的氧化物而使固体质量增大,碳与氧气化合成二氧化碳而使固体质量减小,由于碳减少的质量远小于铁转化为氧化物增加的质量.
所以答案是:(1)0.2g (2)高碳钢 (3)钢中含碳量少,碳减少的质量远小于铁转化为氧化物增加的质量
【考点精析】本题主要考查了根据化学反应方程式的计算的相关知识点,需要掌握各物质间质量比=系数×相对分子质量之比才能正确解答此题.

 快乐5加2金卷系列答案
快乐5加2金卷系列答案【题目】某自然科学兴趣小组,设计了如图所示的装置,用来研究不同金属跟稀硫酸反应的快慢.他们用此装置,选择了甲、乙、丙、丁四种大小相同的金属片,分别与相同体积、相同质量分数的稀硫酸反应,观察30s内从导管口冒出的氢气泡多少,记录在下表中.(“+”越多表示产生的气泡越多).
金属 | 甲 | 乙 | 丙 | 丁 |
氢气泡多少 | ++ | ++++ | +++ | + |
如果四种金属分别是镁、铝、铁、锌中的一种,则丁最有可能是( )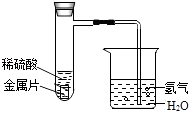
A.镁
B.铝
C.铁
D.锌