题目内容
等质量的下列金属分别与足量的盐酸反应,产生氢气的质量最大的是( )
| A、铁 | B、铝 | C、锌 | D、镁 |
考点:金属的化学性质
专题:金属与金属材料
分析:根据氢气的质量=
×金属质量,利用假设法,假设1g这些金属分别与足量稀盐酸反应生成氢气的质量,再进行比较即可.
| 金属的化合价 |
| 金属的相对原子质量 |
解答:解:
A、铁的相对原子质量56,则1g铁生成
×1g=
g氢气.
B、Al的相对原子质量为27,则1g铝生成
×1g=
g氢气.
C、Zn的相对原子质量为65,则1g锌生成
×1g=
g氢气.
D、Mg的相对原子质量为24,则1g镁生成
×1g=
g氢气.
因为
g>
g>
g>
g,所以铝放出的氢气最多.
故选:B.
A、铁的相对原子质量56,则1g铁生成
| 2 |
| 56 |
| 1 |
| 28 |
B、Al的相对原子质量为27,则1g铝生成
| 3 |
| 27 |
| 1 |
| 9 |
C、Zn的相对原子质量为65,则1g锌生成
| 2 |
| 65 |
| 1 |
| 32.5 |
D、Mg的相对原子质量为24,则1g镁生成
| 2 |
| 24 |
| 1 |
| 12 |
因为
| 1 |
| 9 |
| 1 |
| 12 |
| 1 |
| 28 |
| 1 |
| 32.5 |
故选:B.
点评:本题主要考查考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
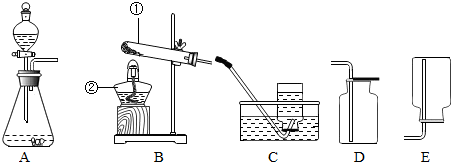
下列实验中,没有发生化学变化的是( )
A、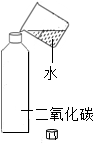 |
B、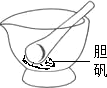 |
C、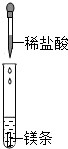 |
D、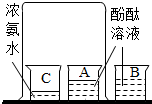 |
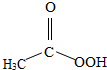 过氧乙酸(CH3COOOH)是常用的消毒剂之一,分子结构如图所示,下列叙述正确的是( )
过氧乙酸(CH3COOOH)是常用的消毒剂之一,分子结构如图所示,下列叙述正确的是( )| A、过氧乙酸属于有机化合物 |
| B、过氧乙酸是由多原子构成的化合物 |
| C、过氧乙酸由碳、氢、氧三个元素组成 |
| D、过氧乙酸中碳、氢、氧原子个数比为2:3:3 |
如图是甲、乙两种固体物质的溶解度曲线,下列说法中正确的是( )
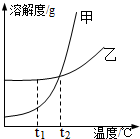

| A、将等质量的甲、乙的饱和溶液分别由t2℃降温至t1℃,析出甲多 |
| B、t2℃时,甲、乙两溶液中溶质的质量分数相等 |
| C、将甲溶液从t2℃降温到t1℃时,一定有晶体析出 |
| D、将t2℃时乙的饱和溶液变为不饱和溶液,可采取降温的方法 |
从金属利用的历史看,先是青铜器时代,而后是铁器时代,铝的利用则是近百年的事,此先后顺序与下列因素有关的是( )
| A、金属的活动性 |
| B、金属的导电性 |
| C、金属在地壳中的含量 |
| D、金属的延展性 |
下列实验操作中,正确的是( )
A、 加热液体 |
B、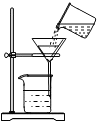 过滤 |
C、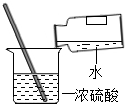 稀释浓硫酸 |
D、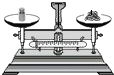 称量 |
作为一名中学生应该有一定的安全防范意识.下列说法正确的是( )
| A、食用用甲醛溶液浸泡的海鲜对人体无害 |
| B、食用酒精和工业酒精的主要成分相同,都可以饮用 |
| C、发生火灾时,应用湿毛巾捂住口鼻,匍匐前进 |
| D、发现煤气泄漏时,立即打开排气扇电源开关 |
下列各物质的名称或俗称与其化学式不一致的是( )
| A、生石灰 氧化钙CaO |
| B、烧碱 纯碱 NaOH |
| C、金刚石 石墨 C |
| D、硫酸铜晶体 胆矾 CuSO4?5H2O |