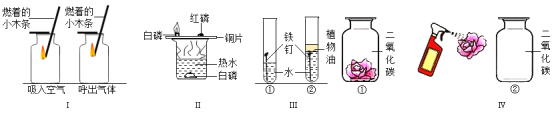
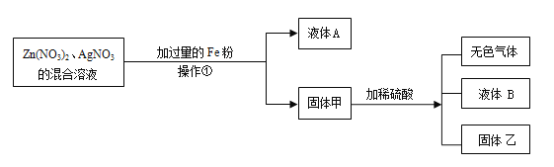
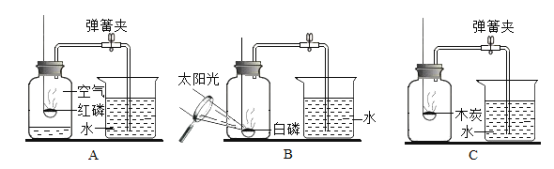
题目内容
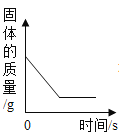
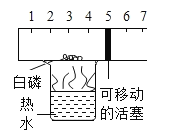
【题目】为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:
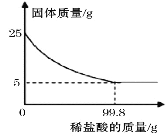
(1)这种贝壳中碳酸钙的质量分数是多少?__________ (碳酸钙的质量分数=![]() )。
)。
(2)25g贝壳与稀盐酸恰好完全反应时,生成二氧化碳的质量多少?__________
【答案】80% 8.8g
【解析】
(1)由图可以看出固体减少了20g,即碳酸钙的质量为20g,所以贝壳中碳酸钙的质量分数为![]() ×100%=80%。
×100%=80%。
(2)设恰好反应时产生二氧化碳的质量为x
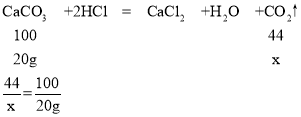
x=8.8g
答:25g贝壳与稀盐酸恰好完全反应时,生成的二氧化碳质量是8.8g。
故答案为:(1)80%;(2)25g贝壳与稀盐酸恰好完全反应时,生成的二氧化碳质量是8.8g。

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目