题目内容
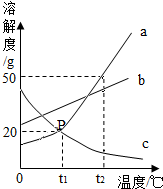
 t2℃时,将100g甲的饱和溶液和100g乙的饱和溶液分别降温到t1℃,对所得溶液的叙述正确的是
t2℃时,将100g甲的饱和溶液和100g乙的饱和溶液分别降温到t1℃,对所得溶液的叙述正确的是
- A.甲、乙都是饱和溶液
- B.所含溶剂质量:甲=乙
- C.溶液质量:甲>乙
- D.溶质质量分数:甲>乙
D
分析:A、根据物质溶解度的变化判断是否饱和;
B、根据t2℃时甲、乙的溶解度分析等质量的饱和溶液中溶剂质量关系,降低温度溶剂的质量不变;
C、根据甲、乙的溶解度随温度变化情况分析降温后溶液的质量变化;
D、根据饱和溶液溶质质量分数的计算,并结合二者的溶解度随温度变化分析.
解答:A、乙的溶解度随温度降低而增大,温度从t2℃降温到t1℃乙的饱和溶液会变成不饱和溶液.甲饱和乙不饱和故错误;
B、t2℃时甲的溶解度大于乙的溶解度,因此该温度下,100g甲、乙的饱和溶液中甲的饱和溶液中溶质质量大,溶剂质量就小,故溶剂甲小于乙,故错误;
C、降低温度甲的溶解度减小会析出晶体而使溶液质量减小,乙的溶解度随温度降低而增大,不会结晶析出故溶液质量不变.所以甲溶液的质量小于乙溶液的质量故错误;
D、乙的溶解度随温度降低而增大不会结晶析出,溶质质量分数不变,等于算式 ×100%,溶解度是t2℃时乙的溶解度;甲的溶解度随温度降低而减小会析出晶体仍然饱和,饱和溶液溶质质量分数=算式
×100%,溶解度是t2℃时乙的溶解度;甲的溶解度随温度降低而减小会析出晶体仍然饱和,饱和溶液溶质质量分数=算式 ×100%,溶解度是t1℃时甲的溶解度.t1℃时甲的溶解度大于t2℃时乙的溶解度,所以若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,溶质质量分数甲大.故正确;
×100%,溶解度是t1℃时甲的溶解度.t1℃时甲的溶解度大于t2℃时乙的溶解度,所以若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,溶质质量分数甲大.故正确;
故选D.
点评:本题很好的考查了对溶解度曲线的了解和应用,容易出错的地方是降温后溶质质量分数的比较,要利用好饱和溶液溶质质量分数的计算公式,并结合溶解度曲线细心分析.
分析:A、根据物质溶解度的变化判断是否饱和;
B、根据t2℃时甲、乙的溶解度分析等质量的饱和溶液中溶剂质量关系,降低温度溶剂的质量不变;
C、根据甲、乙的溶解度随温度变化情况分析降温后溶液的质量变化;
D、根据饱和溶液溶质质量分数的计算,并结合二者的溶解度随温度变化分析.
解答:A、乙的溶解度随温度降低而增大,温度从t2℃降温到t1℃乙的饱和溶液会变成不饱和溶液.甲饱和乙不饱和故错误;
B、t2℃时甲的溶解度大于乙的溶解度,因此该温度下,100g甲、乙的饱和溶液中甲的饱和溶液中溶质质量大,溶剂质量就小,故溶剂甲小于乙,故错误;
C、降低温度甲的溶解度减小会析出晶体而使溶液质量减小,乙的溶解度随温度降低而增大,不会结晶析出故溶液质量不变.所以甲溶液的质量小于乙溶液的质量故错误;
D、乙的溶解度随温度降低而增大不会结晶析出,溶质质量分数不变,等于算式
 ×100%,溶解度是t2℃时乙的溶解度;甲的溶解度随温度降低而减小会析出晶体仍然饱和,饱和溶液溶质质量分数=算式
×100%,溶解度是t2℃时乙的溶解度;甲的溶解度随温度降低而减小会析出晶体仍然饱和,饱和溶液溶质质量分数=算式 ×100%,溶解度是t1℃时甲的溶解度.t1℃时甲的溶解度大于t2℃时乙的溶解度,所以若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,溶质质量分数甲大.故正确;
×100%,溶解度是t1℃时甲的溶解度.t1℃时甲的溶解度大于t2℃时乙的溶解度,所以若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,溶质质量分数甲大.故正确;故选D.
点评:本题很好的考查了对溶解度曲线的了解和应用,容易出错的地方是降温后溶质质量分数的比较,要利用好饱和溶液溶质质量分数的计算公式,并结合溶解度曲线细心分析.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
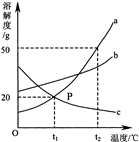 18、右图是a、b、c三种物质的溶解度曲线,请据图回答:
18、右图是a、b、c三种物质的溶解度曲线,请据图回答: 22、如图是a、b、c三种物质的溶解度曲线,请据图回答:
22、如图是a、b、c三种物质的溶解度曲线,请据图回答: (2013?襄城区模拟)t2℃时,将100g甲的饱和溶液和100g乙的饱和溶液分别降温到t1℃,对所得溶液的叙述正确的是( )
(2013?襄城区模拟)t2℃时,将100g甲的饱和溶液和100g乙的饱和溶液分别降温到t1℃,对所得溶液的叙述正确的是( )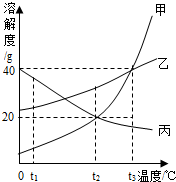 (2012?本溪)甲、乙、丙三种固体物质的溶解度曲线如图所示,根据图示回答下列问题:
(2012?本溪)甲、乙、丙三种固体物质的溶解度曲线如图所示,根据图示回答下列问题: