题目内容
 (2013?西城区二模)我国古代纺织业常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白织物.
(2013?西城区二模)我国古代纺织业常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白织物.Ca(OH)2,K2CO3和KOH的部分溶解度如下表
【资料】①K2CO3+Ca(OH)2═CaCO3↓+2KOH
②Ca(OH)2,K2CO3和KOH的部分溶解度如下表.
| 温度/℃ | 0 | 10 | 20 | 30 | 50 | |
| 溶解度/g | Ca(OH)2 | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 |
| k2CO3 | 107 | 109 | 110 | 114 | 121 | |
| KOH | 97 | 103 | 112 | 126 | 140 | |
110
110
g.溶质的质量分数为50%的KOH溶液属于不饱和
不饱和
溶液(填“饱和”或“不饱和”)(2)某温度时,向一定量的饱和氢氧化钙溶液中加入少量生石灰,恢复到原温度,某些量随时间变化的关系如图所示.则纵坐标可能表示的是
ac
ac
(填序号)a.溶质的质量 b.溶剂的质量 c.溶液的质量 d.溶质的质量分数 e.氢氧化钙的溶解度.
(3)20℃时,将1.38gK2CO3固体放入100g水中,并加入一定量的氢氧化钙,搅拌使其充分反应,恢复到原温度,过滤,得到质量为1.1g的固体.所得滤液中的溶质是
氢氧化钾和氢氧化钙
氢氧化钾和氢氧化钙
,生成碳酸钙的质量是1
1
g.分析:根据表格数据可以知道某温度时物质的溶解度,计算出质量分数为50%的溶液中所含溶质的质量,即可确定溶液是否饱和;根据氧化钙能与水反应放热且氢氧化钙的溶解度随温度升高而减小进行判断纵坐标的含义;根据碳酸钾与氢氧化钙的反应进行有关的计算,据此解答即可.
解答:解:(1)根据表格可以知道,20℃时,100g水中最多可溶解K2CO3的质量是110g,
溶质的质量分数为50%的KOH溶液中,设水的质量是100g,其中含溶质的质量为x,则有
×100%=50%,解得x=100g,观察表格中氢氧化钾在不同温度下的溶解度,0℃最多溶解97g,10℃时最多溶解103g,故溶解100g氢氧化钾的溶液是不饱和溶液,故填:不饱和;
(2)氧化钙能与水反应放出大量的热,氢氧化钙的溶解度随温度的升高而减小,当温度升高时,氢氧化钙在水中的溶解度减小,故溶质质量逐渐减小,当温度逐渐减低时,氢氧化钙的溶解度增大,溶解的溶质逐渐增多,由于氧化钙与水反应消耗一部分水,故溶质的质量比开始时溶质质量要减小,故可以表示溶质质量的变化,溶液是由溶质和溶剂组成的,故可以表示溶液的变化,观察选项,故填:ac;
(3)设1.38g碳酸钾能生成沉淀的质量质量为x
K2CO3+Ca(OH)2═CaCO3↓+2KOH
138 100
1.38g x
=
解得x=1g
而实际得到了1.1g固体,说明加入的氢氧化钙的量有剩余,碳酸钾全部参加反应,生成了氢氧化钾,故溶质为氢氧化钾和氢氧化钙,故填:氢氧化钾和氢氧化钙,1.
溶质的质量分数为50%的KOH溶液中,设水的质量是100g,其中含溶质的质量为x,则有
| x |
| 100g+x |
(2)氧化钙能与水反应放出大量的热,氢氧化钙的溶解度随温度的升高而减小,当温度升高时,氢氧化钙在水中的溶解度减小,故溶质质量逐渐减小,当温度逐渐减低时,氢氧化钙的溶解度增大,溶解的溶质逐渐增多,由于氧化钙与水反应消耗一部分水,故溶质的质量比开始时溶质质量要减小,故可以表示溶质质量的变化,溶液是由溶质和溶剂组成的,故可以表示溶液的变化,观察选项,故填:ac;
(3)设1.38g碳酸钾能生成沉淀的质量质量为x
K2CO3+Ca(OH)2═CaCO3↓+2KOH
138 100
1.38g x
| 138 |
| 1.38g |
| 100 |
| x |
而实际得到了1.1g固体,说明加入的氢氧化钙的量有剩余,碳酸钾全部参加反应,生成了氢氧化钾,故溶质为氢氧化钾和氢氧化钙,故填:氢氧化钾和氢氧化钙,1.
点评:本题考查了溶解度的有关知识,完成此题,可以依据溶解度的有关概念进行.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
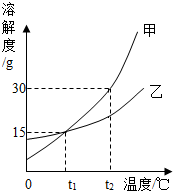 (2013?西城区二模)甲乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
(2013?西城区二模)甲乙两种固体的溶解度曲线如图所示,下列说法正确的是( )