题目内容
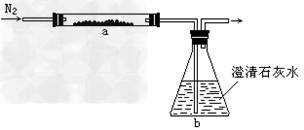
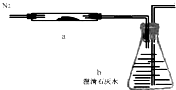 将Fe2O3和纯净的碳粉混合,平铺在反应管a中在瓶盛有足量澄清石灰水按图连接仪器.实验开始时缓慢通入氮气过一段时间后,加热反应管观察到管内发生剧烈反应同时,瓶中的溶液出现白色沉淀待反应反应完成后停止加热仍继续通入氮气直至反应管冷却.此时,管内的混合物变成黑色粉末.回答问题:
将Fe2O3和纯净的碳粉混合,平铺在反应管a中在瓶盛有足量澄清石灰水按图连接仪器.实验开始时缓慢通入氮气过一段时间后,加热反应管观察到管内发生剧烈反应同时,瓶中的溶液出现白色沉淀待反应反应完成后停止加热仍继续通入氮气直至反应管冷却.此时,管内的混合物变成黑色粉末.回答问题:(1)取少量固体溶于足量的稀硫酸,发现有大量的气泡产生,若同时出现
固体全部溶解
固体全部溶解
的现象,则生成的黑色固体全部是铁.(2)实验中通入的气体是纯净干燥的氮气,不用空气的主要原因是
空气中含有氧气会将生成的铁氧化
空气中含有氧气会将生成的铁氧化
.(3)停止加热前是否需要断开和b的连接处?为什么?
不需要,因为氮气不断通入,b瓶中的溶液不会倒吸入a瓶
不需要,因为氮气不断通入,b瓶中的溶液不会倒吸入a瓶
(4)本实验的尾气是否需要处理?如需处理,请回答如何处理,如不需处理,说明理由
需处理,因尾气中有CO,在尾气气出口加一个点燃的酒精灯
需处理,因尾气中有CO,在尾气气出口加一个点燃的酒精灯
.(5)合成氨工业中使用的催化剂铁触媒的成分可表示为xFeO?yFe2O3(其中FeO与Fe2O3质量比为27:20).若用40gFe2O3通过该实验制备出37.6g铁触媒,反应中消耗的纯净碳粉的质量范围是
0.9g~1.8g
0.9g~1.8g
,x:y=3:1
3:1
.分析:根据已有的知识进行分析,铁能与盐酸反应生成氢气,生成的铁在温度高时会被空气中的氧气氧化,实验结束时要持续通入氮气直到冷却,一氧化碳具有毒性,需要进行尾气处理,根据物质的化学式以及反应的质量关系进行计算即可.
解答:解:(1)铁能与盐酸反应生成氢气和易溶于水的氯化亚铁,故填:固体全部溶解;
(2)空气中含有氧气,生成的铁早温度高时能被氧气氧化,故填:空气中含有氧气会将生成的铁氧化;
(3)实验结束后持续通入氮气,不会使液体倒吸,不需要断开,故填:不需要,因为氮气不断通入,b瓶中的溶液不会倒吸入a瓶;
(4)尾气中含有一氧化碳会污染环境,需要进行尾气处理,可以采用点燃的方法,故填:需处理,因尾气中有CO,在尾气气出口加一个点燃的酒精灯;
(5)铁触媒的成分可表示为xFeO?yFe2O3(其中FeO与Fe2O3质量比为27:20,则有
=
,解得
=
,
37.6g铁触媒中含有氧化亚铁的质量为
×37.6g=21.6g,碳与氧化铁反应可以生成一氧化碳也可能生成二氧化碳,
如果是碳与氧化铁反应生成一氧化碳和氧化亚铁,设此时碳的质量为a,
Fe2O3+C
2FeO+CO
12 144
a 21.6g
=
a=1.8g
如果碳与氧化铁反应生成二氧化碳和氧化亚铁,设此时碳的质量为b
2Fe2O3+C
4FeO+CO2
12 288
b 21.6g
=
b=0.9g
所以碳的质量范围是0.9g~1.8g
故填:0.9g~1.8g,3:1.
(2)空气中含有氧气,生成的铁早温度高时能被氧气氧化,故填:空气中含有氧气会将生成的铁氧化;
(3)实验结束后持续通入氮气,不会使液体倒吸,不需要断开,故填:不需要,因为氮气不断通入,b瓶中的溶液不会倒吸入a瓶;
(4)尾气中含有一氧化碳会污染环境,需要进行尾气处理,可以采用点燃的方法,故填:需处理,因尾气中有CO,在尾气气出口加一个点燃的酒精灯;
(5)铁触媒的成分可表示为xFeO?yFe2O3(其中FeO与Fe2O3质量比为27:20,则有
| 72x |
| 160y |
| 27 |
| 20 |
| x |
| y |
| 3 |
| 1 |
37.6g铁触媒中含有氧化亚铁的质量为
| 27 |
| 47 |
如果是碳与氧化铁反应生成一氧化碳和氧化亚铁,设此时碳的质量为a,
Fe2O3+C
| ||
12 144
a 21.6g
| 12 |
| a |
| 144 |
| 21.6g |
a=1.8g
如果碳与氧化铁反应生成二氧化碳和氧化亚铁,设此时碳的质量为b
2Fe2O3+C
| ||
12 288
b 21.6g
| 12 |
| b |
| 288 |
| 21.6g |
b=0.9g
所以碳的质量范围是0.9g~1.8g
故填:0.9g~1.8g,3:1.
点评:本题考查了有关的化学实验注意现象以及根据化学方程式的计算,完成此题,可以依据具体的反应进行.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
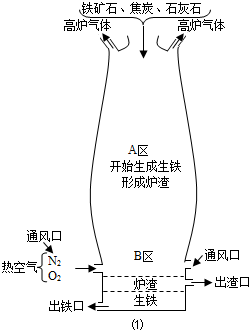
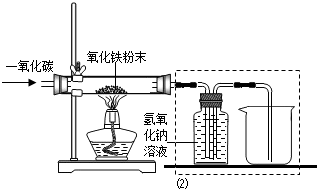
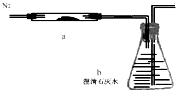 将Fe2O3和纯净的碳粉混合,平铺在反应管a中在瓶盛有足量澄清石灰水按图连接仪器.实验开始时缓慢通入氮气过一段时间后,加热反应管观察到管内发生剧烈反应同时,瓶中的溶液出现白色沉淀待反应反应完成后停止加热仍继续通入氮气直至反应管冷却.此时,管内的混合物变成黑色粉末.回答问题:
将Fe2O3和纯净的碳粉混合,平铺在反应管a中在瓶盛有足量澄清石灰水按图连接仪器.实验开始时缓慢通入氮气过一段时间后,加热反应管观察到管内发生剧烈反应同时,瓶中的溶液出现白色沉淀待反应反应完成后停止加热仍继续通入氮气直至反应管冷却.此时,管内的混合物变成黑色粉末.回答问题: