题目内容
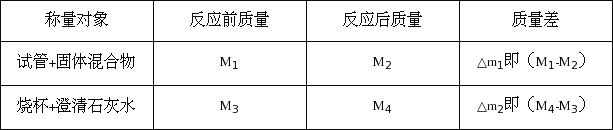
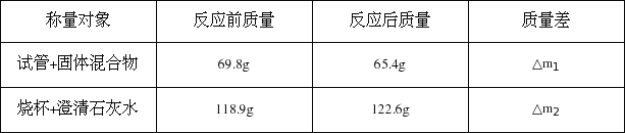
【题目】过氧化氢不稳定会自然分解,久置的过氧化氢溶液,其溶质的质量分数会变小。某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,进行实验。测得相关数据如图9所示:
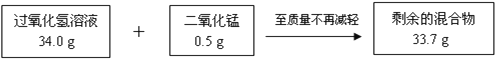
(1)根据质量守恒定律,反应生成氧气的质量为_______。
(2)计算该过氧化氢溶液中溶质的质量分数为_______。
【答案】 0.8g 5%
【解析】依据质量守恒定律计算生成氧气的质量,再根据已知的氧气质量代入化学方程式求得参加反应的过氧化氢的质量,最后可求得过氧化氢溶液中溶质的质量分数。(1) 反应生成氧气的质量=34.0g+0.5g-33.7g=0.8g;设34.0 g过氧化氢溶液中含有过氧化氢的质量为x。
2H2O2MnO22H2O+O2↑
6832
x0.8g![]()
x=1.7g
过氧化氢溶液的溶质的质量分数=![]() ×100%=5%
×100%=5%
答:该过氧化氢溶液中溶质的质量分数为5%。

练习册系列答案
相关题目
【题目】某密闭容器内有X、Y、Z、W四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 | X | Y | Z | W |
反应前质量 | 4 | 1 | 10 | 2 |
反应后质量 | 待测 | 5 | 4 | 8 |
下列说法正确的是![]()
![]()
A. 反应后X的质量为8g
B. Z与W的相对分子质量比一定是1:1
C. 该反应的反应物只有Z
D. 参加反应的X与Z的质量比是2:3