题目内容
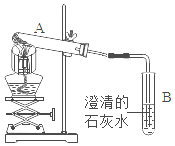
【题目】如图为木炭还原氧化铜的实验装置。请回答下列问题。
(1)试管A中发生反应的化学方程式是_____。
(2)酒精灯加网罩的作用是_____。
(3)实验中,试管B中发生反应的化学方程式是_____
(4)若要使80g氧化铜完全被还原,试管A中实际加入的碳的质量应_____6g。(选填“>”“<”或“=”)
【答案】C+ 2CuO![]() 2Cu + CO2↑集中火焰,提高温度CO2 +Ca(OH)2 ==CaCO3↓+ H2O>
2Cu + CO2↑集中火焰,提高温度CO2 +Ca(OH)2 ==CaCO3↓+ H2O>
【解析】
(1)根据在高温条件下,碳还原氧化铜反应原理书写化学方程式;
(2)酒精灯加网罩能集中火焰,提高温度,据此分析回答;
(3)根据二氧化碳能与氢氧化钙反应原理书写化学方程式;
(4)根据实验的过程分析回答。
(1)在高温条件下,碳能还原氧化铜生成了铜和二氧化碳,所以试管A中发生反应的化学方程式是:C+ 2CuO![]() 2Cu + CO2↑;
2Cu + CO2↑;
(2)在实验时,给酒精灯加网罩的作用是集中火焰,提高温度;
(3)二氧化碳能与氢氧化钙反应生成了碳酸钙和水,所以实验中,试管B中发生反应的化学方程式是:CO2 +Ca(OH)2 ==CaCO3↓+ H2O;
(4)若要使80g氧化铜完全被还原,根据方程式C+ 2CuO![]() 2Cu + CO2↑可知,理论上80g的氧化铜与6g的碳恰好完全反应,由于碳能与试管空气中氧气反应等,试管A中实际加入的碳的质量应>6g。
2Cu + CO2↑可知,理论上80g的氧化铜与6g的碳恰好完全反应,由于碳能与试管空气中氧气反应等,试管A中实际加入的碳的质量应>6g。

 华东师大版一课一练系列答案
华东师大版一课一练系列答案【题目】在介绍氢气的制法时,老师告诉同学们,铝丝与一种可以用铁制容器盛装的溶液反应,也会生成氢气。
(提出问题)与铝丝反应的是什么溶液?
(交流讨论)分析后,大家一致认为该溶液不是稀盐酸或稀硫酸,原因是_____。
同学们决定进一步探究。老师为同学们提供了该溶液。
(查阅资料)含有不同金属离子的溶液在灼烧时会产生不同颜色的火焰
钠 | 钙 | 钾 |
黄色 | 砖红色 | 紫色(透过蓝色钴玻璃) |
(实验探究)
①小强取该溶液于试管中,向其中滴加紫色石蕊溶液,发现紫色石蕊溶液变蓝。
②小明用铂丝蘸取该溶液在酒精灯火焰上灼烧,观察到火焰呈黄色。
③有同学提出应向该溶液中滴加稀盐酸,小美取该溶液于试管中,向其中加入足量的稀盐酸后,没有看到明显现象,这样做是为了排除_____(填离子符号)的干扰。
(实验结论)该溶液为_____溶液。
(交流反思)
①老师告诉同学们,铝与该溶液反应除了生成氢气外,还生成了一种含有A1O2﹣的盐,请写出该反应的化学方程式_____。
②金属铝的化学性质较活泼,而生活中使用的铝制品却耐腐蚀,原因是_____。