题目内容
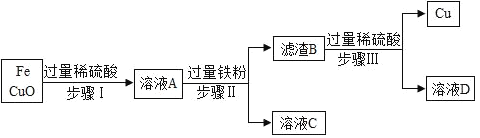
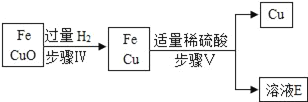
通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,以下是制备精盐的实验方案,各步操作流程如下:
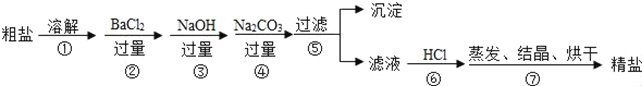
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是_____。
(2)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、_____(填化学式)。
(3)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是_____。
(4)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是_____。
(5)实验所得精盐的质量大于粗盐中NaCl的质量,原因是_____。
(6)某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验研究:称取12g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图。
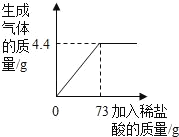
①纯碱恰好完全反应时,生成CO2的质量为_____g
②计算当盐酸与纯碱恰好完全反应时,所得溶液的溶质质量分数是多少?____
练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目