题目内容
【题目】在期末复习课上,李老师在复习部分气体的制取和性质时,向同学们展示了图1,请根据图1回答下列问题: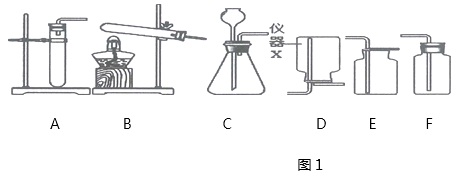
(1)仪器X的名称是;
(2)实验室用高锰酸钾制取O2 , 发生装置应选择 , 化学方程式是:;
(3)若要制备多瓶CO2 , 并在制取过程中便于补充稀盐酸,发生装置应选择 , 收集装置应选择 , 反应的化学方程式为:
(4)如图2是关于物质性质的实验,请回答: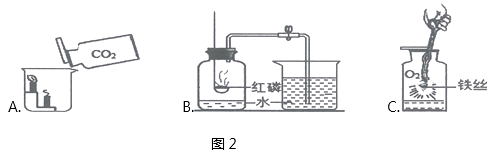
实验A:倾倒足量CO2时观察到的实验现象是;
实验B:测得空气中氧气体积分数偏小的原因可能是(只答一条):;
实验C:集气瓶内放少量水的目的是。
【答案】
(1)集气瓶
(2)B;2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(3)C;E;CaCO3+2HCl=CaCl2+H2O+CO2↑
(4)蜡烛自下而上依次熄灭;装置漏气或红磷量不足等;防止溅落的熔化物炸裂瓶底
【解析】(1)仪器X的名称为集气瓶;(2)实验室用高锰酸钾制取O2 , 反应物的状态为固体,反应条件加热,的怪应选择B作发生装置,化学方程式为2KMnO4![]() K2MnO4+MnO2+O2↑;(3)长颈漏斗可以随时添加液体,所以若要制备多瓶CO2 , 并在制取过程中便于补充稀盐酸,发生装置应选择C;二氧化碳密度比空气大且能溶于水,所以要用向上排空气法收集,实验室制取二氧化碳通常用石灰石和稀盐酸反应完成,方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;(4)倾倒足量CO2时会观察到蜡烛自下而上依次熄灭;测空气中氧气体积分数时若结果偏小,可能是装置漏气或红磷量不足等;铁丝燃烧实验中为防止溅落的熔化物炸裂瓶底,瓶底要预先加少量水。
K2MnO4+MnO2+O2↑;(3)长颈漏斗可以随时添加液体,所以若要制备多瓶CO2 , 并在制取过程中便于补充稀盐酸,发生装置应选择C;二氧化碳密度比空气大且能溶于水,所以要用向上排空气法收集,实验室制取二氧化碳通常用石灰石和稀盐酸反应完成,方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;(4)倾倒足量CO2时会观察到蜡烛自下而上依次熄灭;测空气中氧气体积分数时若结果偏小,可能是装置漏气或红磷量不足等;铁丝燃烧实验中为防止溅落的熔化物炸裂瓶底,瓶底要预先加少量水。
【考点精析】解答此题的关键在于理解氧气与碳、磷、硫、铁等物质的反应现象的相关知识,掌握镁与氧:发出耀眼的白光,放出热量,生成白色固体;铁、铝燃烧要在集气瓶底部放少量水或细砂的目的:防止溅落的高温熔化物炸裂瓶底;铁、铝在空气中不可燃烧,以及对书写化学方程式、文字表达式、电离方程式的理解,了解注意:a、配平 b、条件 c、箭号.

 名校课堂系列答案
名校课堂系列答案【题目】人体内液体的正常pH范围如下表。在这些液体中一定呈酸性的是 ( )
血浆 | 乳汁 | 唾液 | 胆汁 | 胰液 | 胃液 | |
pH范围 | 7.3~7.45 | 6.6~7.6 | 6.6~7.1 | 7.1~7.3 | 7.5~8.0 | 0.9~1.5 |
A.血浆B.胃液C.乳汁D.唾液
【题目】某兴趣小组用KClO3和MnO2制取氧气,试管中固体的质量随时间变化的数据见下表.制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g.
加热时间\min | 0 | t1 | t2 | t3 |
固体质量\g | 28.0 | 23.2 | 18.4 | 18.4 |
(1)共制得氧气g
(2)计算所得氯化钾溶液的溶质质量分数是多少?