题目内容
现有一含杂质的固体氯化钡样品(杂质不溶于水)。取12.5g样品放入烧杯中,然后加入39.6g水使其充分溶解,静置后滤去杂质。取10g滤液加入足量的硝酸银溶液,完全反应后生成沉淀2.87g。试求:(计算结果精确到0.1%)
(1)滤液中溶质的质量分数;
(2)样品中氯化钡的质量分数。
(1)滤液中溶质的质量分数;
(2)样品中氯化钡的质量分数。
解:
(1)设10g滤液中含氯化钡的质量为x。
BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2
208 287
x 2.87g
208:287=x:2.87g x=2.08g
滤液中溶质的质量分数为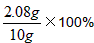 =20.8%
=20.8%
(2)设12.5g样品中含氯化钡的质量为y。
2.08g:(10g-2.08g)=y:39.6g y=10.4g
样品中氯化钡的质量分数为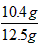 ×100%=83.2%
×100%=83.2%
(1)设10g滤液中含氯化钡的质量为x。
BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2
208 287
x 2.87g
208:287=x:2.87g x=2.08g
滤液中溶质的质量分数为
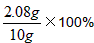 =20.8%
=20.8% (2)设12.5g样品中含氯化钡的质量为y。
2.08g:(10g-2.08g)=y:39.6g y=10.4g
样品中氯化钡的质量分数为
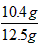 ×100%=83.2%
×100%=83.2% 
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

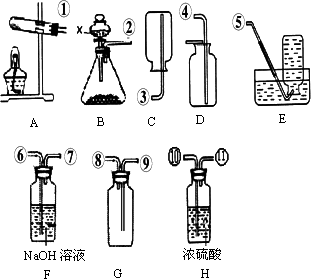
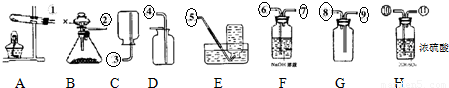
 有下列实验装置示意图:
有下列实验装置示意图: