题目内容
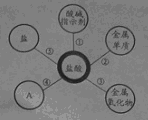
(10分)归纳是学习的重要方法,小红在复习盐酸的性质时归纳出盐酸的五条化学性质(如右图所示,连线表示相互反应)。
(1)为了验证性质①,小红将紫色石蕊试液滴加到盐酸溶液中,溶液变 色;
(2)图中A所代表的物质类别是 ;任举一例写出化学方程式_____________________________________
(3)酸的性质③决定了酸可用于清除铁锈(主要成分是Fe2O3),写出硫酸除铁锈反应的化学方程式是 ;
(4)为了验证性质⑤,有同学想到实验室制取二氧化碳的反应,写出化学方程式___________________________________________________
(5)镁和锌可以用来验证盐酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是 (填序号)。

(1)为了验证性质①,小红将紫色石蕊试液滴加到盐酸溶液中,溶液变 色;
(2)图中A所代表的物质类别是 ;任举一例写出化学方程式_____________________________________
(3)酸的性质③决定了酸可用于清除铁锈(主要成分是Fe2O3),写出硫酸除铁锈反应的化学方程式是 ;
(4)为了验证性质⑤,有同学想到实验室制取二氧化碳的反应,写出化学方程式___________________________________________________
(5)镁和锌可以用来验证盐酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是 (填序号)。
| A.两种金属的大小 | B.盐酸的质量分数 | C.反应容器的大小 | D.温度 |
(1)____红____
(2)______碱________,_______(中和反应即可)_______________
(3)___Fe2O3+3H2SO4==Fe2(SO4)3+3H2O___
(4)__CaCO3+2HCl==CaCl2+H2O+CO2↑__(5)____ABD__
(2)______碱________,_______(中和反应即可)_______________
(3)___Fe2O3+3H2SO4==Fe2(SO4)3+3H2O___
(4)__CaCO3+2HCl==CaCl2+H2O+CO2↑__(5)____ABD__
(1)石蕊遇酸性溶液会变红色,所以将紫色石蕊试液滴加到盐酸溶液中溶液变红,故填:红
(2)综合分析酸的化学性质可知:除去盐酸能与指示剂、金属氧化物、金属、盐反应外还能与碱发生中和反应,故填:碱;中和反应
(3)铁锈的主要成分是氧化铁,与盐酸反应时会生成氯化铁与水,反应的化学方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(4)实验室用大理石和稀盐酸反应制取二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(5)控制变量法就是创设相同的外部条件,因此探究镁和锌与盐酸反应的快慢,需要控制不变的条件就是对反应速度可能有影响的因素,分析知四个因素中只有容器的大小对反应速度无影响.故选ABD
(2)综合分析酸的化学性质可知:除去盐酸能与指示剂、金属氧化物、金属、盐反应外还能与碱发生中和反应,故填:碱;中和反应
(3)铁锈的主要成分是氧化铁,与盐酸反应时会生成氯化铁与水,反应的化学方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(4)实验室用大理石和稀盐酸反应制取二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(5)控制变量法就是创设相同的外部条件,因此探究镁和锌与盐酸反应的快慢,需要控制不变的条件就是对反应速度可能有影响的因素,分析知四个因素中只有容器的大小对反应速度无影响.故选ABD

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目