题目内容
【题目】现有铜与另一种金属R(可能是银、镁、铁中的一种)的混合粉末.欲确定R的成分,请你一起完成:
(1)请将银、镁、铁三种金属的元素符号填写在下列金属活动性顺序表中的相应位置.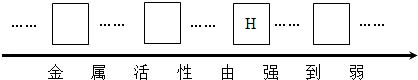
(2)取少量的金属粉末于试管中,逐滴加入稀硫酸,有气泡产生,则R不可能是 .
(3)待不再产生气泡时,再进行(填写一种实验操作方法),得到溶液和铜.然后往溶液中加入洁净的锌片,锌片表面有金属析出,则R是 .
(4)写出金属R与稀硫酸反应的化学方程式 . 该反应的基本类型属于(选填“化合”、“分解”、“置换”或“复分解”)反应.
【答案】
(1)
Mg;Fe;Ag
(2)银(或Ag)
(3)过滤;铁(或Fe)
(4)Fe+H2SO4=FeSO4+H2↑;置换
【解析】解:(1)根据银、镁、铁三种金属的活动性强弱关系镁>铁>氢>银,可判断顺序表最左端空格内为镁,接下来的空格内为铁,最右端为银;(2)铜与另一种金属R的混合粉末能与稀硫酸反应放出氢气,可判断金属R能与酸反应产生氢气,由金属R不可能是金属银;(3)根据操作后把溶液与铜分离开来,可判断该操作为过滤;由于滤液的盐能与锌反应,可判断盐中金属活动性比锌弱,而金属镁的活动性比锌强,因此金属R应为铁;(4)铁与硫酸反应生成硫酸亚铁和氢气,化学方程式为Fe+H2SO4=FeSO4+H2↑;该反应为单质与化合物生成单质与化合物的置换反应;故答案为:(1)Mg,Fe,Ag;(2)银(或Ag);(3)过滤;铁(或Fe);(4)Fe+H2SO4=FeSO4+H2↑;置换.
(1)根据金属活动性顺序,将银、镁、铁三种金属的元素符号填金属活动性顺序表中的相应位置;(2)根据金属与酸反应的规律,由金属粉末与稀硫酸反应,有气泡产生,推断金属R;(3)根据操作后得到溶液和铜的结果,判断所进行的实验操作;根据金属与盐反应规律,由锌片表面有金属析出,推断金属R;(4)根据对金属R的推断,写出与硫酸反应的化学方程式,并对该反应进行分类.



