��Ŀ����
����Ŀ�����ձ��м���20g 1.2%������������Һ������������1.0%��ϡ���ᣬ���ò��������Ͻ��裮ʵ������У���pH��ֽ��βⶨ��ҺpH����Һ��pH��������������仯�������ͼ��ʾ����ش��������⣮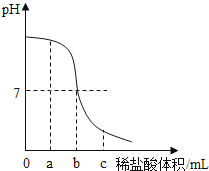
��1����pH��ֽ�ⶨ��ҺpH�IJ����� ��
��2������������Һ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ �� ��������������ΪamLʱ��������Һ�����������������ӷ��ţ�������������cmLʱ�������õ���Һ�м����̪��Һ����Һ��ɫ��
��3�������1.0%��ϡ������ܶ�Ϊ1.0g/cm3 �� ��ͼ��b= ��
���𰸡�
��1����pH��ֽ���ڲ���Ƭ�ϣ��ò�����պȡ����Һ����pH��ֽ�ϣ�Ȼ��ͱ�ɫ���Ƚ�
��2��NaOH+HCl�TNaCl+H2O��Cl����OH������
��3��21.9
����������1����pH��ֽ�ⶨ��ҺpH�IJ����ǽ�pH��ֽ���ڲ���Ƭ�ϣ��ò�����պȡ����Һ����pH��ֽ�ϣ�Ȼ��ͱ�ɫ���Ƚϣ���2������������Һ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ��NaOH+HCl�TNaCl+H2O������ҺpH�ı仯ͼ���֪����a��ʱ����Һ��pH����7����Һ�ʼ��ԣ�˵�����������������ᷴӦ�������Ȼ��ƣ���Һ�л���ʣ����������ƣ�������Һ�е��������ǣ�Cl����OH������C��ʱ����Һ�����ԣ���������ȫ�������ᷴӦ�������Ȼ��ƣ���Һ�л���ʣ������ᣬ�����õ���Һ�м����̪��Һ����Һ����ɫ����3������ҺpH�ı仯ͼ���֪����a��ʱ����Һ��pH����7��˵�����������ƺ�����ǡ���кͣ��������Ƶ�����=20g��1.2%=0.24g
��ϡ��������������Ϊx
NaOH+HCl�TNaCl+H2O
��40 ��36.5
0.24g �� x![]()
x=0.219g��
ϡ���������= ![]() =21.9g����ϡ������ܶ�Ϊ1.0g/cm3 �� ��ϡ��������Ϊ
=21.9g����ϡ������ܶ�Ϊ1.0g/cm3 �� ��ϡ��������Ϊ![]() =21.9cm3 �� ��21.9mL��
=21.9cm3 �� ��21.9mL��
�𰸣���1����pH��ֽ���ڲ���Ƭ�ϣ��ò�����պȡ����Һ����pH��ֽ�ϣ�Ȼ��ͱ�ɫ���Ƚϣ�2��NaOH+HCl�TNaCl+H2O Cl����OH�� �ޣ�3��21.9
�����㾫����������Ĺؼ����������кͷ�Ӧ����Ӧ�õ����֪ʶ�������кͷ�Ӧ����������������κ�ˮ�ķ�Ӧ���Լ�����д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�����⣬�˽�ע�⣺a����ƽ b������ c�����ţ�