题目内容
【题目】化学能转化为电能,在生产、生活中有重要的应用. I.氢氧燃料电池是符合绿色化学理念的新型电池.
图1是氢氧燃料电池的示意图,要配制电池中100mL质量分数为30%的氢氧化钾溶液(密度约为1.290g/cm3),需称量g固体氢氧化钾;电池工作时,H2和O2反应生成水,同时提供电能,溶液的pH(填“变大”“变小”“不变”).
Ⅱ.某学校研究小组对废干电池筒内的黑色物质(可能含有C、MnO2、ZnCl2、NH4C1等)进行研究,实验过程如图2: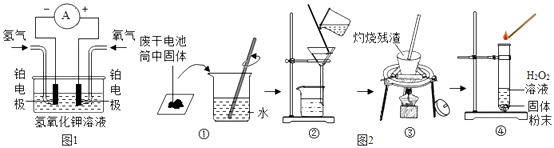
⑴操作①的玻璃棒的作用是 , 操作②的玻璃棒的作用是 .
⑵操作③灼烧滤渣发生反应的化学方程式为是 .
⑶操作④的试管中产生的气体能使带火星的木条复燃,产生该气体的化学方程式是 .
【答案】["38.7","变小","搅拌,加快物质的溶解","引流","C+O2 ![]() CO2","2H2O2
CO2","2H2O2 ![]() 2H2O+O2↑"]
2H2O+O2↑"]
【解析】解:I.氢氧化钾的质量=100mL×1.290g/cm3×30%=38.7g;电池工作时,H2和O2反应生成水,氢氧化钾溶液的浓度较小,碱性减弱,溶液的pH减小;故填:38.7;变小;
Ⅱ.(1)操作①是溶液,在溶解的过程中,玻璃棒的作用是搅拌,加快物质的溶解;操作②是过滤,在过滤操作中玻璃棒的作用是引流;故填:搅拌,加快物质的溶解;引流;(2)氯化锌与氯化铵能溶于水,而二氧化锰和碳粉不溶于水,所以滤渣的成分是二氧化锰和碳粉,灼烧时,碳与氧气反应生成二氧化碳气体;故填:C+O2 ![]() CO2;(3)过氧化氢在二氧化锰的催化作用下分解为水和氧气;故填:2H2O2
CO2;(3)过氧化氢在二氧化锰的催化作用下分解为水和氧气;故填:2H2O2 ![]() 2H2O+O2↑.
2H2O+O2↑.
【考点精析】本题主要考查了书写化学方程式、文字表达式、电离方程式和碳的化学性质的相关知识点,需要掌握注意:a、配平 b、条件 c、箭号;各种单质碳的化学性质却完全相同;1、常温下的稳定性强2、可燃性:完全燃烧(氧气充足),生成CO2;不完全燃烧 (氧气不充足),生成CO;3、还原性:应用:冶金工业;现象:黑色粉末逐渐变成光亮红色,石灰水变浑浊才能正确解答此题.