题目内容
硫酸铁铵[NH4Fe(SO4)2?xH2O]是一种重要铁盐,能在水中解离出NH4+、Fe3+、SO42-。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流 程如下:
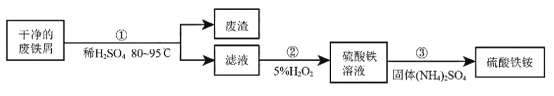
回答下列问题:
(1)步骤①发生反应的方程式是_____________。经检验,废渣是片状石墨,它与金刚石的物理性质有很大差异的原因是___________________。
(2)完成步骤②中的反应2FeSO4+H2O2+____________=Fe2(SO4)3+ 2H2O
(3)如废铁屑表面已生锈(铁锈的主要成分为Fe2O3?xH2O),则步骤①还会发生另外两步反应:
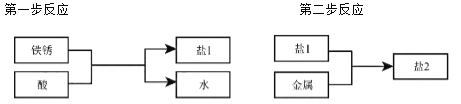
第二步反应中反应物与生成物的化学计量数之比为1:1:3,写出第二步反应的化学方程式: _____ 。
(4)由该实验可知,干净的表面未生锈的废铁屑属于________ (填“纯净物”或“混合物”)。
(5)将步骤③中得到的样品经干燥后加热,失掉全部结晶水,剩余固体的质量为原晶体质量的55.2%,则硫酸铁铵晶体的化学式为_______ (填序号)。
a. NH4Fe(SO4)2?3H2O
b. NH4FeSO4)?6 H2O
c. NH4Fe(SO4)2?9 H2O
d. NH4FeSO4)?12 H2O
(6)完成鉴别硫酸铁和硫酸铁铵两种固体的实验报告。
实验步骤 | 实验现象 | 实验结论 |
_____ | _____ | _____ |
练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目


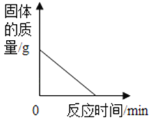 表示向一定量的氧化铁中通入一氧化碳气体并持续高温
表示向一定量的氧化铁中通入一氧化碳气体并持续高温 盐酸和氯化镁的混合溶液中逐滴加入氢氧化钡溶液
盐酸和氯化镁的混合溶液中逐滴加入氢氧化钡溶液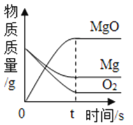 表示镁在氧气中燃烧
表示镁在氧气中燃烧 表示加热氯酸钾与二氧化锰的固体混合物
表示加热氯酸钾与二氧化锰的固体混合物
