题目内容
【题目】某校化学兴趣小组就空气中氧气的含量进行实验探究:【集体设计】化学兴趣小组的同学经过研究讨论,采用燃烧方法除去氧气以后,测定剩余
气体的体积。但首先需要解决两个实际问题:
(1)要能确保消耗其中的氧气,使气体的体积减小,选择什么样的药品就显得很重要。他们应该选择下列物质中的红磷(A.蜡烛 B.红磷 C.木炭)而不能选其他物质,分析理由是
(2)药品的取用量也有相应要求。你认为取用量应达到什么要求?
(3)【设计实验】第一小组同学共同设计了如下图的A、B两套装置。你认为合理的是(填编号)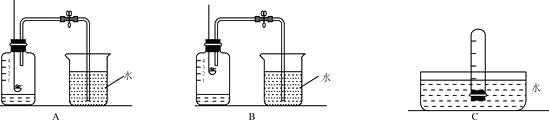
(4)为了确保实验的成功,在装药品之前应该先检查
(5)集气瓶中红磷燃烧的反应符号表达式为
(6)【改进实验】第二小组同学查阅资料得知:白磷不溶于水,露置在空气中容易发生缓慢氧化而引起自燃,而燃烧产生的五氧化二磷会刺激人的呼吸道。于是他们将试管的容积分成五等份,做好标记(如图C)。在试管中加入一小块(足量)白磷,迅速用橡皮塞塞紧试管口,将试管放入热水中,使白磷燃烧。待白磷熄灭并冷却到时室温后,再将试管倒立于盛有水的水槽中,并在水中将橡皮塞取下。C装置的优点是(写一点)
(7)小组A同学用镊子从容器中取出白磷后,准备在滤纸上切割时,B同学立刻阻止了他,指出他的操作不正确,请分析原因
(8)根据上题描述,白磷的物理性质有 , 化学性质有
【答案】
(1)蜡烛、木炭都有气体生成,不能使压强发生明显变化
(2)过量
(3)A
(4)装置气密性
(5)P+O2![]() P2O5
P2O5
(6)环保或减小误差等
(7)白磷的着火点低,在空气中缓慢氧气能引起自燃
(8)白色固体或硬度小等,可燃性
【解析】(1)红磷燃烧消耗氧气,生成物为固体,能使得装置内压强减小,而蜡烛、木炭都有气体生成,不能使压强发生明显变化;(2)为使得测得结果准确,要保证氧气全部消耗,所以取用红磷应过量;(3)实验A和B的区别在于红磷的位置,而这一点与氧气的密度有关,由于氧气的密度大于空气,所以红磷在稍微低的位置更利于反应的进行,也更利于氧气的消耗,所以实验A更合理;(4)为了确保实验成功,实验前要先检查装置气密性,若装置漏气则结果会不准确;(5)红磷燃烧是红磷与氧气反应生成五氧化二磷,表达式为P+O2![]() P2O5;(6)C装置是在装置内引燃白磷,这样白磷不会在装置外的空气中燃烧,也就是白磷燃烧的产物有毒的五氧化二磷不会散失到空气造成环境污染,也节约了药品,所以C装置的优点是环保,同时也利于实验的结果的准确;(7)白磷的着火点低,在空气中缓慢氧气能引起自燃,故不能在滤纸上切割白磷;(8)由题中描述可知,白磷为白色固体,硬度小,这些性质都属于物理性质,白磷具有可燃性为化学性质。
P2O5;(6)C装置是在装置内引燃白磷,这样白磷不会在装置外的空气中燃烧,也就是白磷燃烧的产物有毒的五氧化二磷不会散失到空气造成环境污染,也节约了药品,所以C装置的优点是环保,同时也利于实验的结果的准确;(7)白磷的着火点低,在空气中缓慢氧气能引起自燃,故不能在滤纸上切割白磷;(8)由题中描述可知,白磷为白色固体,硬度小,这些性质都属于物理性质,白磷具有可燃性为化学性质。
根据测定空气中氧气体积分数的原理分析,测定氧气体积分数时选择能与空气中氧气反应的物质,且生成物为固体,使得装置内因氧气反应消耗压强变小,再根据补充的水或活塞移动的体积确定氧气的体积。在做该实验时,要保证装置气密性良好,否则会使得结果不准确。

 阅读快车系列答案
阅读快车系列答案