题目内容
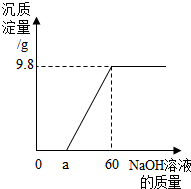
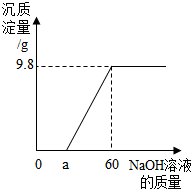 小明在做铁置换硫酸铜的实验时,发现铁钉表面有气泡产生,经测定,知是硫酸铜中混入了少量稀硫酸,为测定溶液的组成情况,取100克混合溶液,向其中加入质量分数为20%的NaOH溶液,产生的沉淀与所加入NaOH溶液的质量关系如图:
小明在做铁置换硫酸铜的实验时,发现铁钉表面有气泡产生,经测定,知是硫酸铜中混入了少量稀硫酸,为测定溶液的组成情况,取100克混合溶液,向其中加入质量分数为20%的NaOH溶液,产生的沉淀与所加入NaOH溶液的质量关系如图:
(1)oa段所发生的反应是NaOH与混合溶液中的______反应.
(2)混合溶液中H2SO4的质量分数是多少?
解:(1)根据氢氧化钠既能与硫酸反应也能与硫酸铜反应且氢氧化钠与硫酸反应时没有现象发生,因此OA段的反应是2NaOH+H2SO4═Na2SO4+2H2O;
(2)由图象可知在OA发生氢氧化钠与硫酸反应,从a到60g段则是氢氧化钠与硫酸铜的反应,
设生成9.8g产点需氢氧化钠的质量为x
2NaOH+CuSO4═Na2SO4+Cu(OH)2↓
80 98
20%×x 9.8g
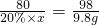
x=40g
故与稀硫酸反应的氢氧化钠溶液质量是60g-40g=20g
设硫酸的质量是y
2NaOH+H2SO4═Na2SO4+2H2O
80 98
20g×20% y
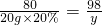
y=4.9g
故混合溶液中H2SO4的质量分数是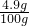 ×100%=4.9%
×100%=4.9%
故答案为:(1)硫酸;(2)混合溶液中H2SO4的质量分数是4.9%;
分析:分析关系图可知,向混合溶液中滴加氢氧化钠溶液先与硫酸反应,待混合溶液中硫酸完全反应后开始与硫酸铜溶液发生反应,因此在计算生成最大沉淀量时所加入的氢氧化钠溶液的总质量时,应该考虑到上述的反应情况,即所加入的氢氧化钠溶液的总质量为与硫酸反应的溶液和与硫酸铜反应的溶液质量和.
点评:正确地分析图象是解题的关键.分析沉淀的质量与所滴入NaOH溶液的质量关系曲线时,曲线起点表明混合溶液中硫酸恰好完全反应,曲线折点表明硫酸铜恰好与氢氧化钠完全反应.
(2)由图象可知在OA发生氢氧化钠与硫酸反应,从a到60g段则是氢氧化钠与硫酸铜的反应,
设生成9.8g产点需氢氧化钠的质量为x
2NaOH+CuSO4═Na2SO4+Cu(OH)2↓
80 98
20%×x 9.8g
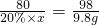
x=40g
故与稀硫酸反应的氢氧化钠溶液质量是60g-40g=20g
设硫酸的质量是y
2NaOH+H2SO4═Na2SO4+2H2O
80 98
20g×20% y
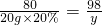
y=4.9g
故混合溶液中H2SO4的质量分数是
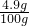 ×100%=4.9%
×100%=4.9%故答案为:(1)硫酸;(2)混合溶液中H2SO4的质量分数是4.9%;
分析:分析关系图可知,向混合溶液中滴加氢氧化钠溶液先与硫酸反应,待混合溶液中硫酸完全反应后开始与硫酸铜溶液发生反应,因此在计算生成最大沉淀量时所加入的氢氧化钠溶液的总质量时,应该考虑到上述的反应情况,即所加入的氢氧化钠溶液的总质量为与硫酸反应的溶液和与硫酸铜反应的溶液质量和.
点评:正确地分析图象是解题的关键.分析沉淀的质量与所滴入NaOH溶液的质量关系曲线时,曲线起点表明混合溶液中硫酸恰好完全反应,曲线折点表明硫酸铜恰好与氢氧化钠完全反应.

练习册系列答案
相关题目
 (2008?海淀区一模)小东和小明收集了两个形状、大小、轻重和硬度均不同的易拉罐,如图所示.他们很想知道每个易拉罐的材料成分,于是展开了以下探究过程.
(2008?海淀区一模)小东和小明收集了两个形状、大小、轻重和硬度均不同的易拉罐,如图所示.他们很想知道每个易拉罐的材料成分,于是展开了以下探究过程.
 小明在做铁置换硫酸铜的实验时,发现铁钉表面有气泡产生,经测定,知是硫酸铜中混入了少量稀硫酸,为测定溶液的组成情况,取100克混合溶液,向其中加入质量分数为20%的NaOH溶液,产生的沉淀与所加入NaOH溶液的质量关系如图:
小明在做铁置换硫酸铜的实验时,发现铁钉表面有气泡产生,经测定,知是硫酸铜中混入了少量稀硫酸,为测定溶液的组成情况,取100克混合溶液,向其中加入质量分数为20%的NaOH溶液,产生的沉淀与所加入NaOH溶液的质量关系如图: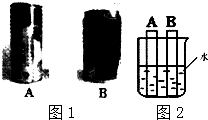 小东和小明收集了两个形状、大小、轻重和硬度均不同的易拉罐,如图1所示.他们很想知道每个易拉罐的材料成分,于是展开了以下探究过程.
小东和小明收集了两个形状、大小、轻重和硬度均不同的易拉罐,如图1所示.他们很想知道每个易拉罐的材料成分,于是展开了以下探究过程.