题目内容
将5g一氧化碳和二氧化碳的混合气体与足量的氧化铜加热充分反应后得到6.4g金属铜,求原混合气体中碳元素的质量分数?
解:设混合气体中CO的质量为x
CO+CuO Cu+CO2
Cu+CO2
28 64
x 6.4g
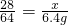
解得,x=2.8g
所以二氧化碳的质量为 5g-2.8g=2.2g
原混合气体中碳元素的质量分数= ×100%=36%
×100%=36%
分析:根据已知量6.4g金属铜,设出一氧化碳的质量,根据CO+CuO Cu+CO2 求出一氧化碳的质量,再求出二氧化碳的质量,然后根据两种气体中碳元素的质量分数,求出碳元素的质量,比上气体的总质量即是混合气体中碳元素的质量分数.
Cu+CO2 求出一氧化碳的质量,再求出二氧化碳的质量,然后根据两种气体中碳元素的质量分数,求出碳元素的质量,比上气体的总质量即是混合气体中碳元素的质量分数.
点评:在解此类题时,首先分析题中的反应原理,然后结合题中方程式中的等量关系进行分析解答需要的数据,再结合题意进行计算.
CO+CuO
 Cu+CO2
Cu+CO2 28 64
x 6.4g
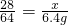
解得,x=2.8g
所以二氧化碳的质量为 5g-2.8g=2.2g
原混合气体中碳元素的质量分数=
 ×100%=36%
×100%=36%分析:根据已知量6.4g金属铜,设出一氧化碳的质量,根据CO+CuO
 Cu+CO2 求出一氧化碳的质量,再求出二氧化碳的质量,然后根据两种气体中碳元素的质量分数,求出碳元素的质量,比上气体的总质量即是混合气体中碳元素的质量分数.
Cu+CO2 求出一氧化碳的质量,再求出二氧化碳的质量,然后根据两种气体中碳元素的质量分数,求出碳元素的质量,比上气体的总质量即是混合气体中碳元素的质量分数.点评:在解此类题时,首先分析题中的反应原理,然后结合题中方程式中的等量关系进行分析解答需要的数据,再结合题意进行计算.

练习册系列答案
相关题目
 是,下列说法不正确的是
是,下列说法不正确的是