题目内容
【题目】某研究小组对自动充气气球(示意图如图)进行下列探究。
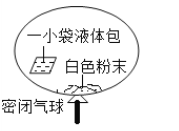
[查阅资料]该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。
(1)为检验气体是二氧化碳,可选用___________(填试剂名称)、
探究一:液体包内溶液酸碱性的探究
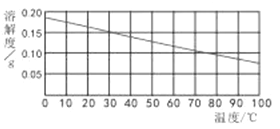
(2)室温时,用pH试纸测得溶液的pH=3,则该溶液呈______性。
探究二:白色粉末成分的探究
[猜想与假设]甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠。
[设计并进行实验]
(3)将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想________(填“正确”或“不正确”)、
(4)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%盐酸(装置如图),记录如表:
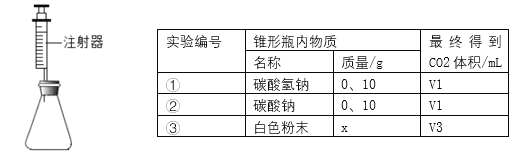
实验①的化学方程式为______________;表中x=___;V1___V2(填“>”、“<”或“=”)、
[分析并得出结论]
(5)白色粉末是__________、
【答案】(1)氢氧化钙溶液(2)酸(3)不正确(4)0.10g,> ;(5)碳酸氢钠
【解析】(1)检验二氧化碳用到的是澄清的石灰水,将气体通入澄清的石灰水中,若澄清的石灰水变浑浊,则证明该气体是二氧化碳;(2)pH<7的溶液呈酸性,现用pH试纸测得溶液的pH=3,则该溶液呈酸性;(3)由于碳酸钙难溶于水,根据实验现象“少量白色粉末放入水中搅拌,固体全部溶解,”说明甲同学的猜想错误;(4)碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式表示为NaHCO3+ HCl ==NaCl + H2O + CO2↑;利用化学方程式,根据碳酸钠与二氧化碳反应的质量比、碳酸氢钠与二氧化碳反应的质量比可知:等质量的质量碳酸钠和碳酸氢钠分别与稀盐酸反应,碳酸氢钠反应产生的二氧化碳的量更多,即V1>V2;要判断白色固体是碳酸钠还是碳酸氢钠,那么取相同质量的固体与稀盐酸反应,比较产生的二氧化碳的量即可,故x=0.10g;(5)根据表中二氧化碳的体积与锥形瓶内物质质量关系,实验③与实验①相同,故该白色物质的碳酸氢钠。

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案【题目】某化学兴趣小组的同学利用下图装置制取并收集一瓶二氧化碳气体,请和他们一起完成以下实验探究。

(1)写出标号①的仪器名称__________。
(2)实验室制取一瓶二氧化碳气体,应选用的收集装置为__________(填序号),反应的化学方程式为__________。
(3)化学兴趣小组的同学对反应后废液中溶质的成分进行进一步探究。
【提出问题】 废液中的溶质含有哪些物质?
【查阅资料】 氯化钙溶液呈中性。
【猜想与假设】 猜想①:废液中的溶质只有氯化钙;
猜想②:废液中的溶质是氯化钙和__________(填化学式)。
【设计并进行实验】 I.为验证上面两种猜想哪种正确,甲小组的同学从下面A~E五种药品中选择合适的一种进行实验,证明了猜想②是正确的。他们选择的药品不可能是__________。
A.紫色石蕊试液 B.无色酚酞试液 C.锌粒 D.氧化铁粉末 E.氢氧化钠溶液
Ⅱ.乙小组用一种钠盐溶液进行实验,也证明了猜想②是正确的,请完成下面的实验报告。
实验操作 | 实验现象 | 实验结论 |
取少量反应后的废液于试管中,加入足量_______(填化学式)溶液,振荡。 | ____________ | 猜想②正确 |
【探究反思】:实验产生的污染深受人们重视,我们要利用恰当的方法对废液进行处理,实行无害化排放,从源头上消除对环境的污染。