题目内容
【题目】由碳酸钾和碳酸钠组成的混合物中碳元素的质量分数为10%,则该混合物中氧元素的质量分数为( )
A.30%
B.40%
C.50%
D.60%
【答案】B
【解析】设混合物中碳酸钾的质量为X,碳酸钠的质量为Y,相对分子质量=(相对原子质量×原子个数)之和,碳酸钾的相对分子质量为:138;碳酸钠的相对分子质量为:106, ![]() 所以碳酸钾中碳元素的质量为 X×(12÷138×100%);碳酸钠中碳元素的质量为 Y×(12÷106×100%);混合物中碳元素的质量分数为{X×(12÷138×100%+y×(12÷106×100%))+}÷(X+y)×100%=10%;X/Y=161/159;可认为碳酸钾的质量为161g,碳酸钠的质量为159g。该混合物中氧元素的质量分数={161g×(48÷138×100%+159×(48÷106×100%))+}÷(161+159)×100%=40%
所以碳酸钾中碳元素的质量为 X×(12÷138×100%);碳酸钠中碳元素的质量为 Y×(12÷106×100%);混合物中碳元素的质量分数为{X×(12÷138×100%+y×(12÷106×100%))+}÷(X+y)×100%=10%;X/Y=161/159;可认为碳酸钾的质量为161g,碳酸钠的质量为159g。该混合物中氧元素的质量分数={161g×(48÷138×100%+159×(48÷106×100%))+}÷(161+159)×100%=40%
所以答案是:B。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】小明同学在实验室做课外活动探究实验时,发现了一个非常奇怪的现象,当他把煤炭放在如下图容器中燃烧时,发现紫红色的高锰酸钾溶液变成了无色。请你跟她一起探究原因。
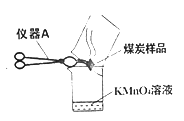
(1)【提出问题】什么使紫红色的高锰酸钾溶液褪色的?
(2)【查阅资料】煤炭燃烧能够产生二氧化碳,而且煤炭中有硫元素,还会燃烧生成二氧化硫气体。
(3)【猜想与假设】a、甲同学假设____________,同学假设:二氧化硫能使紫红色的高锰酸钾溶液褪色的。
(4)【实验与结论】两位同学为了验证自己的猜想,设计以下实验进行验证,为点燃煤炭还须用到的一种玻璃仪器是_________________。
实验步骤 | 实验现象 | 实验结论 |
甲实验:取5mL稀高锰酸钾溶液于一支试管中,________,观察现象。 | _______________________ | 甲同学假设不成立 |
乙实验:_______________并将二氧化硫气体通入试管,观察现象。 | 稀高锰酸钾溶液褪色 | 乙同学假设___ |
(5)【反思评价】我国的能源结构中,燃煤约占70%,比重很大。你觉得如何减少煤燃烧产生的污染物 。