题目内容
实验室欲配制1000g溶质质量分数为4%的氢氧化钠溶液.配制步骤为:
(1)计算:需氢氧化钠固体
(2)称量:用质量为23.1g的烧杯作称量容器,在托盘天平上称取氢氧化钠固体时,盛有氢氧化钠固体的烧杯应放在
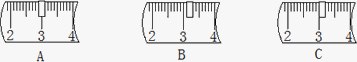
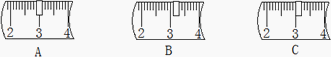
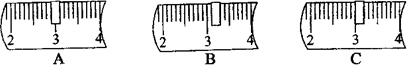
并在下列标尺中选出能正确表示游码位置的选项

(3)溶解:将氢氧化钠固体溶于水,用
(4)存放:等氢氧化钠溶液冷却后,把其转移到玻璃试剂瓶中,贴上标签.存放时塞紧瓶子的塞子要选择
(5)假如在该实验中,你配制的氢氧化钠溶液质量分数小于4%,请分析一个造成小于4%的可能因素:
(1)计算:需氢氧化钠固体
40
40
g,水960
960
mL(水的密度是1g/cm3).(2)称量:用质量为23.1g的烧杯作称量容器,在托盘天平上称取氢氧化钠固体时,盛有氢氧化钠固体的烧杯应放在
左
左
盘(填:“左”或“右”),在下表所列的砝码中,选出所需砝码(打“√”表示选用):| 砝码/g | 100 | 50 | 20 | 20 | 10 | 5 |
| 打“√”表示选用 |
B
B
(填字母)
(3)溶解:将氢氧化钠固体溶于水,用
玻璃棒
玻璃棒
搅拌,使氢氧化钠全部溶解.(4)存放:等氢氧化钠溶液冷却后,把其转移到玻璃试剂瓶中,贴上标签.存放时塞紧瓶子的塞子要选择
胶塞
胶塞
(填“玻璃塞”或“胶塞”)(5)假如在该实验中,你配制的氢氧化钠溶液质量分数小于4%,请分析一个造成小于4%的可能因素:
称量时氢氧化钠和砝码放反了,左码右物(合理均可)
称量时氢氧化钠和砝码放反了,左码右物(合理均可)
.分析:(1)利用溶液的溶质质量分数,计算配制一定质量分数的一定量溶液需要溶质的质量和溶剂的体积,溶质质量=溶液质量×溶液的溶质质量分数,溶剂质量=溶液质量-溶质质量,溶剂体积=
;
(2)根据使用托盘天平称取氢氧化钠质量的操作方法:左物右码、砝码的选用、游码的调整分析解答;
(3)溶解操作常用玻璃棒搅拌,加速固体溶解;
(4)氢氧化钠与玻璃中的成分二氧化硅可发生反应,据此解答;
(5)导致溶液中氢氧化钠质量分数小于4%的可能原因是:溶质少了(左码右物称量;溶质有杂质;游码不在零位置就调节天平平衡)或溶剂多了(量水时仰视读数;烧杯或试剂瓶中有水),据此分析.
| 溶剂质量 |
| 密度 |
(2)根据使用托盘天平称取氢氧化钠质量的操作方法:左物右码、砝码的选用、游码的调整分析解答;
(3)溶解操作常用玻璃棒搅拌,加速固体溶解;
(4)氢氧化钠与玻璃中的成分二氧化硅可发生反应,据此解答;
(5)导致溶液中氢氧化钠质量分数小于4%的可能原因是:溶质少了(左码右物称量;溶质有杂质;游码不在零位置就调节天平平衡)或溶剂多了(量水时仰视读数;烧杯或试剂瓶中有水),据此分析.
解答:解:(1)配制1000g溶质质量分数为4%的氢氧化钠溶液需要氢氧化钠固体质量=1000g×4%=40g;
则需要水的质量=1000g-40g=960g,水的密度是1g/cm3,合960mL;
(2)称取氢氧化钠时为防止腐蚀天平的托盘,放在烧杯内根据“左物右码”的原则放在左边托盘内进行称取,氢氧化钠固体与烧杯的总质量为40g+23.1g=63.1g;所以选择砝码时应选:50g和10g砝码各一个;游码应移动至3.1g处,游码左侧示数为游码质量,图中A表示2.9g、B表示3.1g、C表示3.0g;
(3)溶解过程中用于搅拌以加快物质溶解的仪器为玻璃棒;
(4)氢氧化钠与玻璃反应生成硅酸钠,俗称水玻璃,有很强的粘性,时间长了就把玻璃瓶和瓶塞粘住了,所以用玻璃塞会打不开,存放时塞紧瓶子的塞子要选择胶塞;
(5)导致溶液中氢氧化钠质量分数小于4%的可能原因有两种:溶质少或溶剂多,溶质少了(左码右物称量;溶质有杂质;游码不在零位置就调节天平平衡)或溶剂多了(量水时仰视读数;烧杯或试剂瓶中有水),
故答案为:(1)40;960;
(2)左;
B;
(3)玻璃棒;
(4)胶塞;
(5)称量时氢氧化钠和砝码放反了,左码右物(合理均可).
则需要水的质量=1000g-40g=960g,水的密度是1g/cm3,合960mL;
(2)称取氢氧化钠时为防止腐蚀天平的托盘,放在烧杯内根据“左物右码”的原则放在左边托盘内进行称取,氢氧化钠固体与烧杯的总质量为40g+23.1g=63.1g;所以选择砝码时应选:50g和10g砝码各一个;游码应移动至3.1g处,游码左侧示数为游码质量,图中A表示2.9g、B表示3.1g、C表示3.0g;
(3)溶解过程中用于搅拌以加快物质溶解的仪器为玻璃棒;
(4)氢氧化钠与玻璃反应生成硅酸钠,俗称水玻璃,有很强的粘性,时间长了就把玻璃瓶和瓶塞粘住了,所以用玻璃塞会打不开,存放时塞紧瓶子的塞子要选择胶塞;
(5)导致溶液中氢氧化钠质量分数小于4%的可能原因有两种:溶质少或溶剂多,溶质少了(左码右物称量;溶质有杂质;游码不在零位置就调节天平平衡)或溶剂多了(量水时仰视读数;烧杯或试剂瓶中有水),
故答案为:(1)40;960;
(2)左;
| 砝码/g | 100 | 50 | 20 | 20 | 10 | 5 |
| 打“√”表示选用 | √ | √ |
(3)玻璃棒;
(4)胶塞;
(5)称量时氢氧化钠和砝码放反了,左码右物(合理均可).
点评:本题较细致的考查了天平的使用和溶液配制的误差分析等知识,能结合溶质的质量分数正确分析错误操作引起的后果是解答的关键.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目