题目内容
【题目】下图体现了有关碱的化学性质,请回答问题:
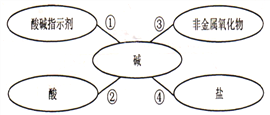
⑴甲同学将酚酞试液滴入Ca(OH)2溶液中,观察到溶液变红,得出结论:Ca(OH)2溶液呈____性。
⑵乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到的实验现象是_____________。
⑶请写出用氢氧化钠溶液吸收有害气体二氧化硫的反应方程式_____________。
⑷丙同学将碳酸钠溶液加入Ca(OH)2溶液中,发现溶液变浑浊,发生的反应化学方程式是________,该反应属于_________反应(填基本反应类型)。
【答案】 碱 溶液由红色变为无色(或红色褪去) 2NaOH + SO2 = Na2SO3+ H2O Na2CO3 + Ca(OH)2 = CaCO3↓ + 2NaOH 复分解反应
【解析】本题考查了碱的通性。根据碱的通性进行分析。
(1)酚酞试液遇碱变红色,将酚酞试液滴入Ca(OH)2溶液中,观察到溶液变红,说明Ca(OH)2溶液呈碱性;
⑵乙同学将过量的稀盐酸加入到甲同学所得溶液中,盐酸与氢氧化钙反应生成氯化钙和水,溶液的碱性减弱,恰好完全反应时,溶液呈中性,盐酸过量时,溶液呈酸性,观察到的实验现象是溶液由红色变为无色(或红色褪去);
⑶氢氧化钠溶液与二氧化硫反应生成亚硫酸钠,反应方程式是2NaOH + SO2 = Na2SO3+ H2O;
⑷碳酸钠溶液加入Ca(OH)2溶液中,反应生成碳酸钙和氢氧化钠,反应化学方程式是Na2CO3 + Ca(OH)2 = CaCO3↓ + 2NaOH;该反应是由两种化合物互相交换成分,生成另外两种化合物,属于复分解反应。

【题目】某同学向一定质量的石灰石中加入7.3%的稀盐酸来制取二氧化碳,测得反应过程中溶液的pH与加入的稀盐酸的关系如右图所示。

(1)该同学能收集到的二氧化碳的质量多少?(写出计算过程)
(2)该同学把制取气体后的废液过滤,向滤液中加入10.6%的Na2CO3溶液,测得加入的Na2CO3溶液与产生的沉淀数据如下:
Na2CO3溶液质量/g | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
沉淀质量/g | 0 | 1 | n | 3 | 4 | 5 | m |
则m= 。加入10gNa2CO3溶液时发生反应的化学方程式是 。
请在右图中画出向废液中加入Na2CO3溶液时加入的Na2CO3溶液与产生的沉淀的曲线。