题目内容
【题目】NaCl、KNO3两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
A.20℃时,NaCl的溶解度为31.6 g
B.将10℃时两物质饱和溶液升温至30℃,溶液中溶质的质量分数都增大
C.为了除去NaCl固体中混有的少量KNO3 , 可加热将其完全溶解后,再通过降温结晶、过滤来除之
D.50℃时,将50g KNO3加入50g水中,充分溶解后溶液的质量为92.75g
【答案】D
【解析】A、20℃时,NaCl的溶解度为36g,31.6g错误;故选项错误;A不符合题意;
B、将10℃时两物质饱和溶液升温至30℃,溶液中溶质的质量分数都不变,增大错误,因为NaCl、KNO3两种固体物质的溶解度,都是随温度升高而增大,故选项错误;B不符合题意;
C、为了除去NaCl固体中混有的少量KNO3,可加热将其完全溶解后,再通过降温结晶、过滤来除之错误,还有一部分硝酸钾;故选项错误;C不符合题意;
D、50℃时,将50g KNO3加入50g水中,充分溶解后溶液的质量=42.75g+50g=92.75g,故选项正确;D符合题意.
故答案为:D.
A. 在溶解度曲线图上,横坐标是温度,纵坐标是溶解度;
B. 将10℃时两物质饱和溶液升温至30℃,两种物质的溶解度变大,溶质的质量不变,溶液中溶质的质量分数都不变;
C. 为了除去NaCl固体中混有的少量KNO3,可加热将其完全溶解后,再通过降温结晶、过滤来除之;因为硝酸钾的溶解度随温度的降低而迅速减小,而氯化钠的溶解受温度的影响很小,所以降温析出晶体几乎全是硝酸钾,过滤得硝酸钾固体;
D. 50℃时,将50g KNO3加入50g水中,溶解硝酸钾42.75g,42.75g+50g即为溶液的质量.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】小韬买了一瓶钙片说明书某些地方模糊不清.于是她做实验探究:取2片钙片加入50g盐酸溶液,两者恰好完全反应(假设钙片中其他成分不与盐酸溶液反应),测得玻璃杯中剩余物质的总质量(m)与反应时间(t)的关系如图所示.
XX钙片 |
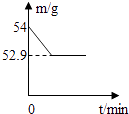
请你帮小韬计算
(1)反应后产生气体的质量g.
(2)所用盐酸溶液中溶质的质量分数.
(3)请你通过计算,在标签的最后一行补充上相应内容: 含量:碳酸钙g/片 可提供钙元素g/片




